|
<解説記事ダウンロード>
<概要>
多細胞生物に対する放射線作用の重要な部分は、それを構成する個々の細胞に対する影響、特にその細胞死に由来する。細胞死には増殖死(分裂死)と間期死とがある。 高線量の放射線を照射した場合には、DNA分子以外の標的に対する傷害によって直接その細胞を死にいたらしめる。この型の細胞死を間期死と呼び、個体の中枢神経死がこれに属する。 増殖死は、細胞核内のDNAに対する傷害によるもので、細胞の分裂能の壊失を意味している。 また、放射線照射により目で見ることのできる細胞の変化が見られなくても、DNAに障害が起こると、ガンなどの晩発傷害が現れる可能性や生殖細胞への放射線効果として、遺伝的影響の可能性も考慮されるべきである。 <更新年月> 2001年03月 (本データは原則として更新対象外とします。)
<本文>
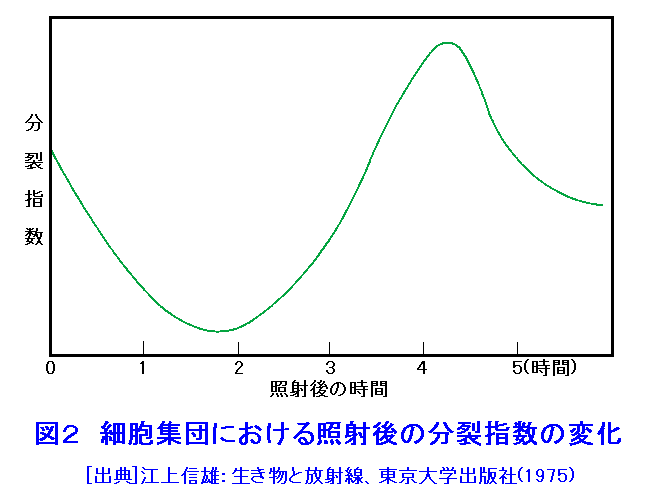
放射線によって引き起される高等動物への障害は、生体内の細胞への影響が根本にある。細胞に対する放射線作用の中で、細胞死は、1)小線量で起こる、2)その影響が細胞集団、個体にまで及ぶ、という二つの理由で特に重要である。 細胞分裂が盛んで分化の程度の低い細胞の放射線感受性が高い傾向にあることは、Bergonie-Tribondeauの則(哺乳動物細胞の放射線感受性の違いを説明する一般則)としてよく知られている。これは、現象として 1)細胞分裂の遅れ、2)照射直後には細胞の物質代謝等は特に見るべき変化はないのに分裂できなくなること、即ち数回の分裂を経た後に分裂が停止してしまい、死細胞が生ずることなどが知られている。これを増殖死(または分裂死)という。 受けた線量が大きいか、または小さい場合でも細胞の種類によっては、照射を受けた細胞そのものが分裂を経ることなしに死滅する場合がありこれを間期死という。 また、放射線により染色体異常や遺伝子突然変異が、生殖細胞で起これば遺伝的影響になり、体細胞で起これば晩発障害としてガンを生ずる可能性がある。この他に細胞は形態・代謝・生理的性質等に照射の影響が現れるが、一時的な変化で時間と共に元へ戻るものと影響が後まで残るものがある。さらに、細胞分裂周期の中の各段階で放射線感受性が変化する。 (1) 増殖死(reproductive death) 細胞における死は、個体の死の定義とは必ずしも一致しない。増殖死とは、本来は増殖能を持つ細胞がその分裂能を失うことを意味する。従って、たとえ細胞が正常に代謝を続けていても、1つの細胞が培養によってコロニーとして目に見える細胞集団に増殖しない、つまり増殖能力を失えば増殖死と見なされる。培養細胞集団を考えたときに、放射線の線量の増加と共に死ぬ細胞の数が増えてコロニーの数が減少する。しかし、充分な高線量を照射しても全ての細胞を死滅させることは困難である。このことから標的説が提出された。放射線のエネルギーは細胞内に一様に分布するのではなく、偶然に標的(DNA)にエネルギー吸収が起こったとき(ヒットしたとき)に初めて細胞死が起こるとしたものである。これで培養細胞における放射線効果の全てを説明できるわけではないが、多くの部分を理解することができる。 さて、標的説に基づき、コロニー形成能を指標にすると線量−生存率曲線を説明することができる。ここで細胞内の標的を一つとし、1つのヒットで増殖死が生じる場合には、線量−生存率曲線の勾配は片対数グラフ上で直線になる。一方、同じ感受性を持つ複数(N個)の標的の全てが一つ以上のヒットを受けないと細胞が死なないと考えると、線量−生存率曲線の低線量部分ではなだらかな肩を持ち、ある線量以上では勾配が直線になる( 図1 )。図1中、Nは標的数(外挿値という)に相当し、D0は標的の大きさに逆比例し、Dqは障害からの回復の程度を示す値である。 しかし、最近は線量−生存率曲線がガン治療などの実用的な利用も説明できるよう、その精度を高めた 直線-二次曲線モデルが使われるようになった。放射線治療を施す場合、比較的低い線量が使われるが、標的説によるとこの線量域での線量−生存率の実験値は、理論値と適合せず、とくに標的数が多くなった場合にはその違いは顕著となる。そこで、実験で得た線量−生存率曲線をαD+βD2の式で近似して、線量−生存率曲線を説明したものが直線−二次曲線モデルである。ここで、低線量部分では直線部分が主でなだらかな肩ができる。高線量では二次曲線が主となる。これによってガン治療の際、多分割照射の有効性を説明できるようになった。図1中で低LET放射線照射時の線量−生存率曲線は、図1中のBに対応し、高LET放射線照射ではAに対応する。 (2) 分裂遅延 動物体内で細胞分裂をしている細胞集団に放射線を照射すると、一時的に分裂像が減少しその後急激に分裂像が増加する( 図2 )。これには体の全体的な細胞分裂の制御も関与するが、培養細胞でも同様の現象がみられる。これは照射によって細胞周期のG2期でM期への移行が阻止(ブロック)されて細胞がここで蓄積することによる。これはG2ブロックと呼ばれ、その結果分裂遅延が起こる。分裂遅延が起きる機構はまだ明らかではないが、おそらく細胞分裂に必要なタンパク質の合成が、照射によって阻害されることによると考えられている。G2ブロックは一時的で、解除されると蓄積した細胞がM期にどっと入り、分裂指数が上昇し細胞分裂の同調化がみられる。 (3) 間期死(interphase death) 照射された細胞が分裂することなく死滅する現象をいう。間期死を起こすには一般的に非常に高い線量(数十グレイ)が必要であるが、リンパ系細胞や若い卵母細胞では少ない線量(ラット、マウスの出生直後の卵母細胞:0.2〜1グレイ)で間期死を起こすなど、細胞によって間期死を起こすのに必要な線量が異なる。また、間期死を起こす細胞はそれが分裂していなくても、盛んに分裂していても起こる。後者の場合には細胞周期の一サイクルよりも短時間に起こる。分裂死はDNAに対する傷害によって起こると考えられているが、間期死を引き起す標的分子が何なのかは不明である。しかし、例えば膜系の傷害、核構造の変化、ATP合成の阻害などのように、分裂死の場合とは異なり、DNA以外への傷害により間期死が起こるという考え方が多い。 (4) 形態学的変化 細胞の死は、大きく分けてネクローシス(壊死)とプログラムされた死(アポトーシス)の2つに分けられる。ネクローシスは、傷害を受けた細胞の受動的・病理的死で、細胞の膨化・ミトコンドリアの変化が起こる。これに対し、生理的な死のシグナルに反応し一定のプログラムに従って起きる細胞死をアポトーシスいい、形態学的にも生化学的にもネクローシスとは区別されている。例えばリンパ球は放射線感受性が高く、比較的少線量で間期死を起こすが、これはアポトーシスである。アポトーシスは能動的・生理的な細胞死で、細胞の縮小・核の断片化・核内クロマチンの凝縮・細胞の分断化(アポトーシス小体の形成)・マクロファージなどによるアポトーシス小体の貪喰消化などが起こる。胎内被ばくにおける奇形発生では、発生異常を起こすような傷を持った細胞がアポトーシスによって排除される仕組みが存在する。この他に顕微鏡的にはミトコンドリアの形態的変化や数の減少、紡錘体の大きさの減少、中心体の増加なども報告されている。しかし、これらは放射線を照射してかなりの時間が経過した後に現れるものが多く、細胞が死に向かう原因なのか結果なのかは明らかでない。 (5) 生理生化学的変化 ここでは膜系の透過性の変化と、細胞内の代謝と酵素活性への影響について考える。本来、生体中の膜は半透膜であるが、その濃度勾配に抗してエネルギーを使って能動輸送を行い、物質の分布を選択的に変えている。この結果、細胞内部は外部と比べてカリウムの濃度が高く、ナトリウムは外部が高くなっている。放射線照射の結果、これらのイオン透過性が高まり細胞中にナトリウムの増加とカリウムの消失をもたらす。また、放射線は種々の代謝系にも影響を与える。例えば、DNA代謝を見ると照射によってDNA合成が低下したり、DNA分解酵素量が増加する。また、核やミトコンドリアでの酸化的リン酸化の抑制が起こったり、脂質代謝の上昇が見られる。放射線による酵素活性の変化は、多くの細胞や組織でいろいろな酵素が調べられている。 <図/表> 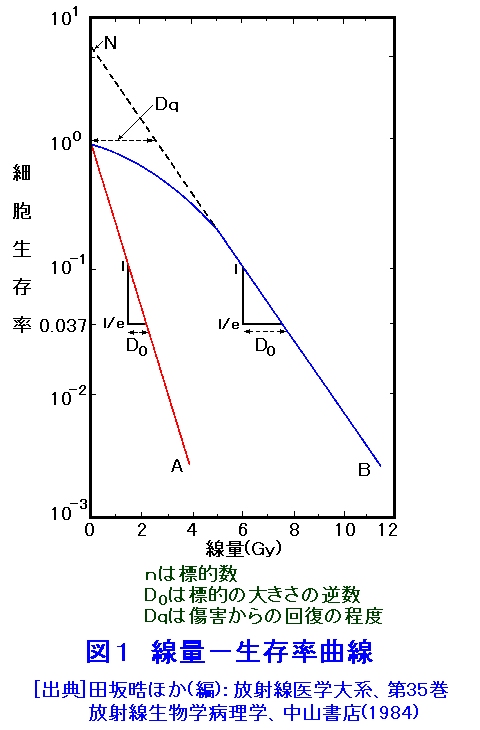
<関連タイトル> 細胞の構成 (09-02-02-01) 体細胞と組織構成 (09-02-02-04) 生殖細胞の構成 (09-02-02-05) 放射線の細胞系への影響 (09-02-02-08) 被ばく線量と生物学的効果 (09-02-02-13) 放射線の細胞分裂に及ぼす影響 (09-02-02-16) <参考文献> (1)江上信雄(著):生き物と放射線、東京大学出版会(1975) (2)田坂晧ほか(編):放射線医学大系 第35巻 放射線生物学病理学、中山書店(1984) (3)Eric J.Hall、浦野宗保(訳):放射線医学のための放射線生物学、篠原出版(1979) (4)菅原努(監修)、青山喬(編著):放射線基礎医学、金芳堂(2000) (5)坂本澄彦:放射線生物学、秀潤社(1998)
|

