|
<解説記事ダウンロード>
<概要>
がん(癌)の放射線治療は、外部照射治療、小線源治療(腔内照射治療・組織内照射治療)、放射性同位元素(RI)投与治療の大略3種類の手法に分類される。これらは併用あるいは使い分けて、多くの種類のがんに対し、単独療法として、あるいは集学治療の一環として適用されている。外部照射に用いられる放射線は主にX線、γ線、電子線で、ほとんどすべてのがんが何らかの形で治療の対象となりうるが、比較的頻度の高いがんのうち、頭頸部がん、肺がん、乳がん、食道がん、子宮がんなどが対象となることが多い。密封小線源治療に用いられる放射線のほとんどはRIから放射されるγ線で、舌がんや子宮がんなど、外部から比較的容易に到達できる部位のがんが対象となる。RI投与治療に用いられるRIは、もっぱら放射性ヨウ素で、対象となるのは甲状腺がんである。近年は外部照射放射線として陽子線、重粒子、パイ中間子、中性子線など新しい放射線による治療が行われている。 <更新年月> 2009年02月
<本文>
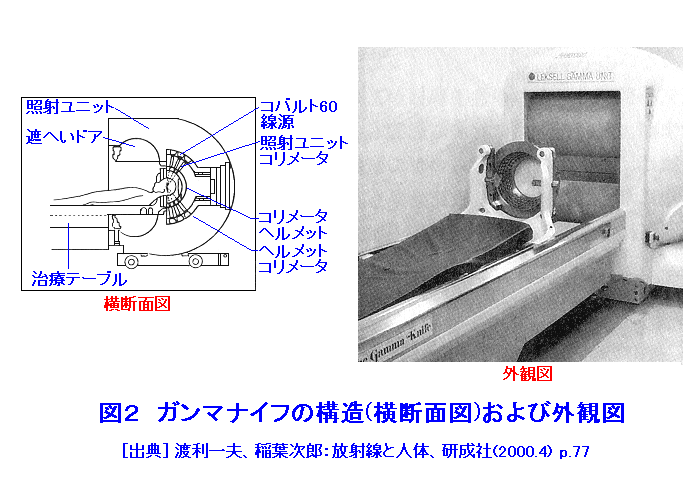
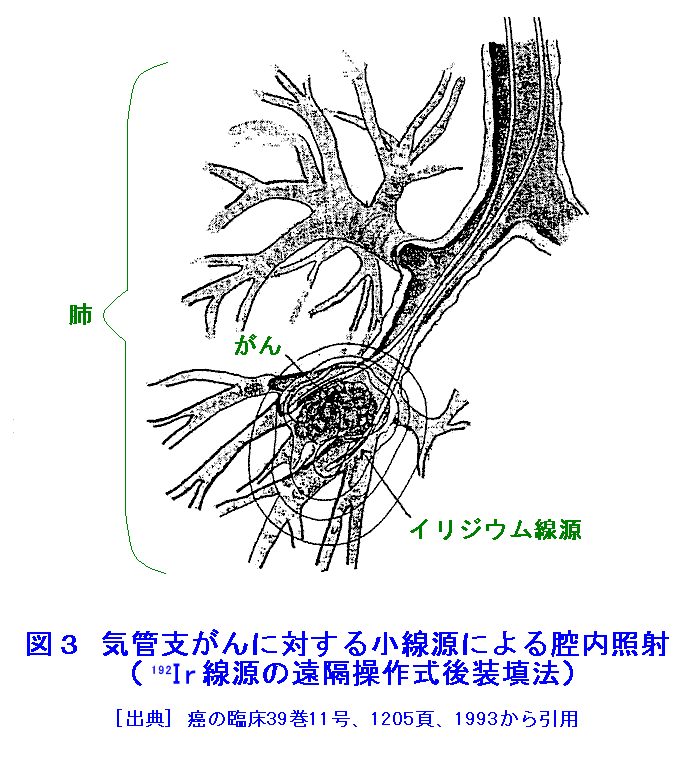
放射線治療の手法には大きく分けて外部照射による治療、密封小線源による治療、放射性同位元素(RI)を用いた治療の3つがあり、対象とする疾患に応じて使い分けられている。また、外部照射治療の変法として、対象病巣を露出させて行う開創照射、術中照射や、特殊な放射線を用いる粒子線治療なども一部で行われている。 1.外部照射治療 人体の外部から病巣に的を絞って放射線を照射する治療法の総称である。放射線としては現在、一般的にはX線、γ線(この2つは物理学的には光子(フォトン)という同一のものである)、電子線の3種類が用いられている。 X線は、古くはX線管(診断用のものと基本的に同一構造)から得られる数十万電子ボルトのエネルギーのものを利用していたが、最近は線型加速器(リニアックまたはライナックという)による数百万ないし千数百万電子ボルトの高エネルギーのものが一般的である。エネルギーが高いため、深部の病巣にも効率よく適用でき、現在の放射線外部照射治療の主役となっている。 γ線は、コバルト60から発生する百万電子ボルト(1MeV)程度のエネルギーのものを利用するのが一般的である。直線加速器から得られるX線ほどエネルギーが高くないので、深部病巣の治療には最適とはいえないが、病巣が比較的浅く、空気を含んだ空洞が複雑に入り組んでいる頭頸部腫瘍(主に耳鼻咽喉科で扱う腫瘍)や、浅部のリンパ節転移巣や脊椎などの骨への転移巣の治療に適している。 電子線は、現在では線型加速器によるものがほとんどであるが、最近まではベータトロンが用いられていた。電子線はその性質上、限られた深さまでしか到達しないので、主として皮膚がんなど表在性腫瘍の治療に適用される。 外部照射の場合、とくに深部の病巣にエネルギーを集中させて部位選択性を向上させるためには、複数の方向から同一の病巣に的を絞って照射する多門照射法を行うのが一般的である。たとえば、体の中心部にある病巣に対して、異なる方向のX線ビームを照射することにより、これらのビームが交差した病巣部に大きな効果を与え、それ以外の正常組織への影響を低減させることが可能となる(図1)。多門照射を発展させた方法として、身体の病巣を中心として、線源を回転させながら照射する回転照射法があり、これには360°回転する全回転照射と、一定の範囲を往復する振子照射とがある。これらを更に発展させた方法として、CT(コンピュータ・トモグラフィ)による画像診断とコンピュータによる線量分布計算とを組み合わせて、病巣の立体的形状に合わせて放射線を集中する「原体照射法」がある。 また、外部照射の場合、1回ごとの照射治療が比較的簡単に行えるので、照射スケジュールに工夫を加えることにより、生物学的選択性を向上させることが可能である。一般的に腫瘍細胞は、ある量の放射線を受けたときに、正常細胞に比べてわずかながら大きな障害を受け、また、それから回復するのに要する時間がわずかながら長いといわれている。したがって放射線の照射を複数回に分割することにより、腫瘍組織と正常組織の障害の差を増幅して、臨床的治癒をより容易に達成することができる。どのような分割スケジュールが適当であるかは、腫瘍そのものの性質、存在部位、用いる放射線の種類など、多くの要因が関与するが、現在では総線量60Gyを6週間かけて30回に分割して与えるというのが標準とされている。 ラジオサージャリー(放射線手術)のひとつとしてガンマナイフがある。コリメーターを通して出てくるガンマ線を集中させて照射効果を上げる方法である。その鋭利さからナイフにたとえられ、手術が難しい脳や血管近くの腫瘍の治療に適用されている(図2参照)。 2.小線源治療 (1)腔内照射 腫瘍が子宮、膣、食道、直腸、口腔、鼻腔など、外部から比較的容易に到達できる体腔に存在する場合は、放射線源(密封小線源)を腫瘍組織の周囲に配置することにより部位選択性を向上させることができる。これを腔内照射という。例として子宮頸部がんに対する照射の場合、子宮腔内と、子宮頸部をはさむ位置に線源を一定時間配置して、局所ならびに近傍に進展した腫瘍細胞に放射線照射を行う。 用いられる放射線源(γ線源)としてはコバルト60、セシウム137、イリジウム192などが代表的であり、線源の形状や放射線エネルギーなどに応じて使い分けられる。また、これらの線源を必要な位置に配置・固定するために、線源形状と病巣位置・形状に合わせた器具(アプリケータ)が種々考案されている。腔内照射の例を図3に示す。 腔内照射の最大の利点は、外部照射に比べて高い部位選択性が得られることであるが、反面、線源から離れた場所に十分なエネルギーが与えられないため、大きく進展した腫瘍に対しては有効ではない。また、手技が煩雑であり、部位によっては患者の苦痛も大きいため、くり返しの照射が難しい。したがって、腔内照射そのものを単独で適用することはあまりなく、外部照射などと組み合わせて実施することがほとんどである。 多くの場合、腔内照射は高線量率・短時間照射で行われるが、低線量率で数時間ないし1日程度の時間を費やし照射を行い、外部照射の項で述べた腫瘍組織と正常組織の障害の差の増幅による生物学的選択性の向上をあわせて試みることもある。また、腔内照射は線源を直接取り扱う必要上、医療スタッフ(医師、放射線技師、看護師など)の被ばくが問題であるが、最近ではアプリケータをセットした後、線源の最終的配置を遠隔操作で行う「遠隔操作式後装填法(Remote After Loading System:RALS)」が普及し、医療スタッフの被ばくをゼロにすることができるようになった。 (2)組織内照射 舌がんなど、体の表面に限局して存在する腫瘍の場合、外科的に線源を腫瘍組織内部に埋め込んで治療を行うことがある。これを「組織内照射」という。用いられる放射線源(γ線源)としては、イリジウム192、金198などが代表的である。 この照射法は適用できる疾患が限られてはいるが、放射線治療の持つ部位・生物学的選択性の2つをフルに生かした治療法ということができ、舌がんなどは針状のラジウム226を1週間程度、腫瘍組織内部および近傍に刺入しておくだけで、舌の機能を保全したまま完全に治癒させることが可能である。 患者の苦痛と医療スタッフの被ばくが欠点といえるが、後者については「後装填法」の適用による改良が試みられている。 3.RIを用いた治療 特定の臓器組織に選択的に集まる性質を持った放射性物質のうち、β線やα線を放出するものは、その臓器組織だけに選択的に放射線障害を起こす。この現象を利用して、バセドウ病やがんの治療が行われている。 バセドウ病(甲状腺機能亢進症)の場合は、ヨウ素が甲状腺に選択的に取り込まれることを利用し、β線を放出する放射性ヨウ素(131I)を185ないしは370M(106)Bq(5〜10mCi)投与して治療を行う。アメリカのある大統領はこの方法で執務を中断することなくバセドウ病の治療を行った。また、病巣の組織や細胞にRIを送り込み、そのRIからの放射線照射で治療する方法は、RIミサイル療法と呼ばれている。 がんの場合は、金属・非金属元素では適当なものが見つかっていない。しかし、がんに特異的に結合するモノクローナル抗体をあらかじめ作っておき、これにβ線やα線を放出する核種を標識して用いればよい。現在用いられている核種は131I、90Y(放射性イットリウム)等であるが、α放射体を用いる研究も進んでいる。 4.開創照射(術中照射) 主に膵臓がん・胆道がんなどの腹部深部がんに対して、外科手術で病巣を露出させた上で放射線照射を行うことがある。これを開創照射または術中照射という。照射すべき範囲を実際に目で見、手でさわって決定し、部位選択性をより確実にすることができるのが利点で、一般には表在性腫瘍の外部照射と同様、電子線が用いられることが多い。厳密には、単純に病巣を露出させて照射する場合を開創照射、外科的腫瘍切除と併用して照射を行う場合を術中照射と呼んで区別する。 一般の放射線治療に用いられる放射線は、X線、γ線、電子線の3つであるが、最近ではこれ以外の放射線による治療も試みられている。陽子線と重粒子線は、限られた施設ではあるが半ば実用化されており、強い期待が寄せられている。陽子線の利用は筑波大学陽子線医学利用研究センターで、重粒子線の利用は(独)放射線医学総合研究所で治療が進められている。 また、ホウ素中性子捕獲療法(BNCT:Boron Neutron Capture Therapy)といって、原子炉で発生する熱中性子を用いる方法もあり、(独)日本原子力研究開発機構と京都大学原子炉実験所で行われている。 (前回更新:2003年9月) <図/表> 
<関連タイトル> 重粒子線照射によるがんの治療 (08-02-02-01) 放射線によるがんの治療(特徴と利点) (08-02-02-03) RI小線源によるがん治療 (08-02-02-04) 中性子を用いたがんの治療(中性子捕捉療法) (08-02-02-05) パイ中間子によるがん治療 (08-02-02-07) ラジオサージャリー(ガンマナイフ、リニアックナイフなど) (08-02-02-10) RIミサイル療法 (08-02-02-11) <参考文献> (1)新版看護学全書:「放射線看護技術」メディカルフレンド社(1989) (2)放射線医学大系:「放射線治療学総論」中山書店(1983) (3)E.J.Hall:Radiobiology for Radiologist,Third Ed.Lippincott(1988) (4)特集号「放射線治療の進歩」、「癌の臨床」、39巻 No.11(1993) (5)高島力ほか(編)、有水昇(監修):標準放射線医学第5版、医学書院(1999.12) (6)木村修治、河野通雄(編):放射線治療学第2版、金芳堂(1996.6) (7)青山喬(編著):放射線基礎医学、第9版、金芳堂(2000.3) (8)筑波大陽子線医学利用研究センター: (9)放射線医学総合研究所:重粒子線がん治療臨床試行の状況について、(1998年3月25日) (10)放射能医学総合研究所:新しい放射線治療−重粒子線治療をお受けになる方のために(1998.6) (11)渡利一夫、稲葉次郎:放射線と人体、研成社(2000.4) (12)放射線医学総合研究所:HIMAC NEWS、放医研NEWS、No.82、2003年9月号
|

