|
<解説記事ダウンロード>
<概要>
放射線治療は、がん細胞のDNAに直接・間接的に作用してがん細胞を殺滅する治療法で、がんの初期から緩和医療まで広く対応できる。治療法は、放射線源を体外に置く外部放射線療法と、放射線源を体内に挿入、刺入又はがん細胞中に沈着させる内部放射線療法がある。外部療法には、光子線(X線、γ線)と粒子線(電子、中性子、陽子、重粒子)が用いられる。内部療法には密封RIのγ線及び非密封RIのβ線が利用される。外部療法では、光子線利用が今日の放射線治療の主流を占め、がんの正確な照射と周辺組織の被ばく低減のため、三次元原体放射線療法(3D−CRT)、強度変調放射線療法(IMRT)、画像誘導放射線療法(IGRT)、定位放射線療法(STI)等の技術が開発されている。高LED(線エネルギー付与)の粒子線(陽子線、重粒子線)を利用する治療は、光子線では対応困難な悪性腫瘍の治療の為に開発が進められているが、今は「先進医療」として臨床研究の段階にある。内部療法は、密封線源を腔内や組織内に挿入し、又はがん表面に密着させて照射治療する。非密封線源の131I,89Sr,90Yは、注射や服用で体内に摂取し、がん細胞に沈着してβ線でがんを照射するので内療法ともいう。 <更新年月> 2016年01月
<本文>
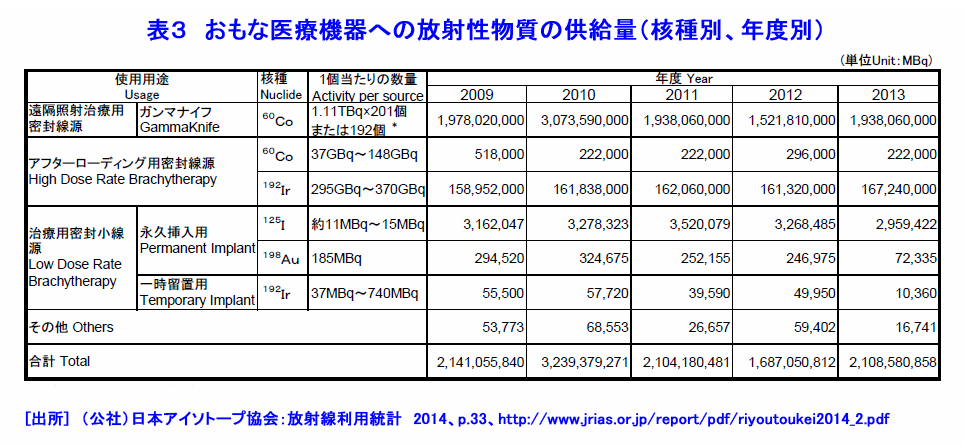
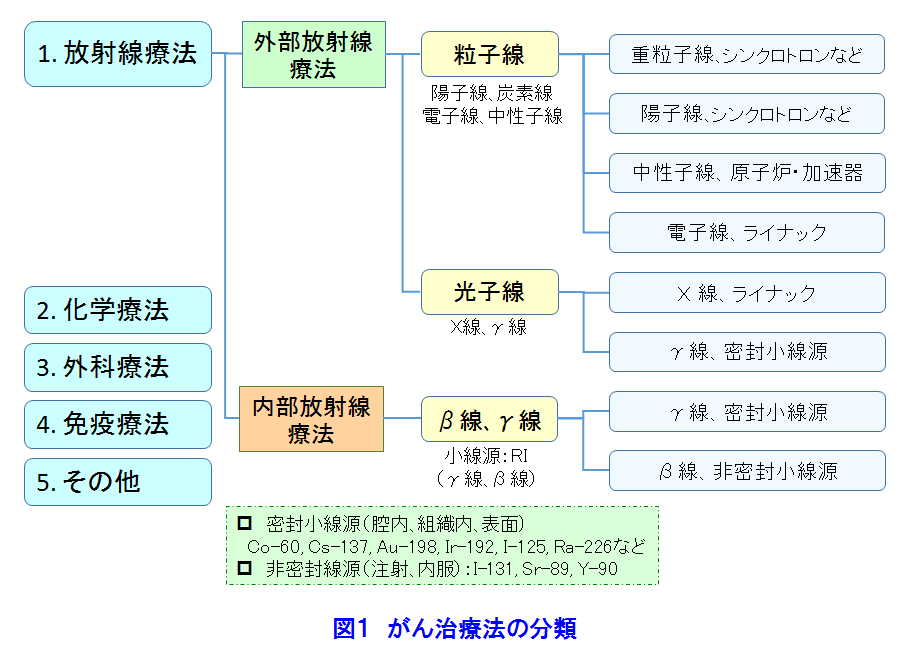
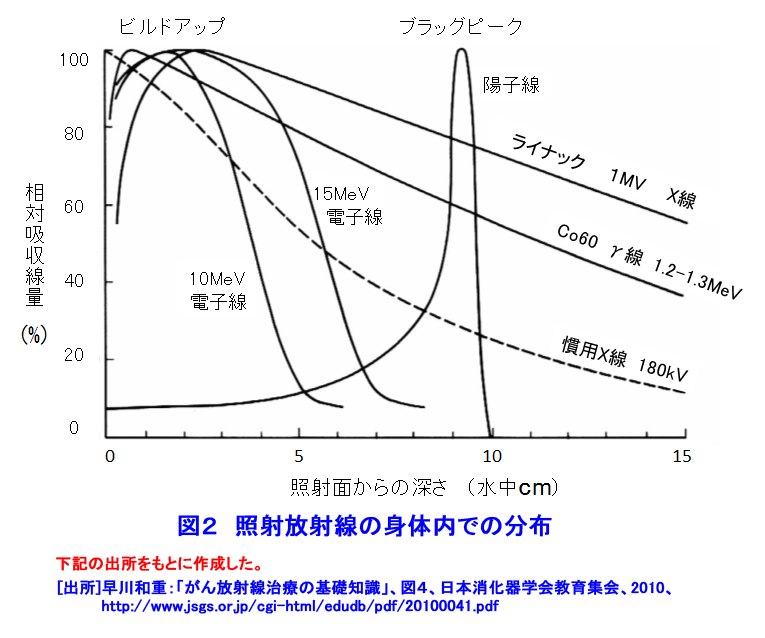
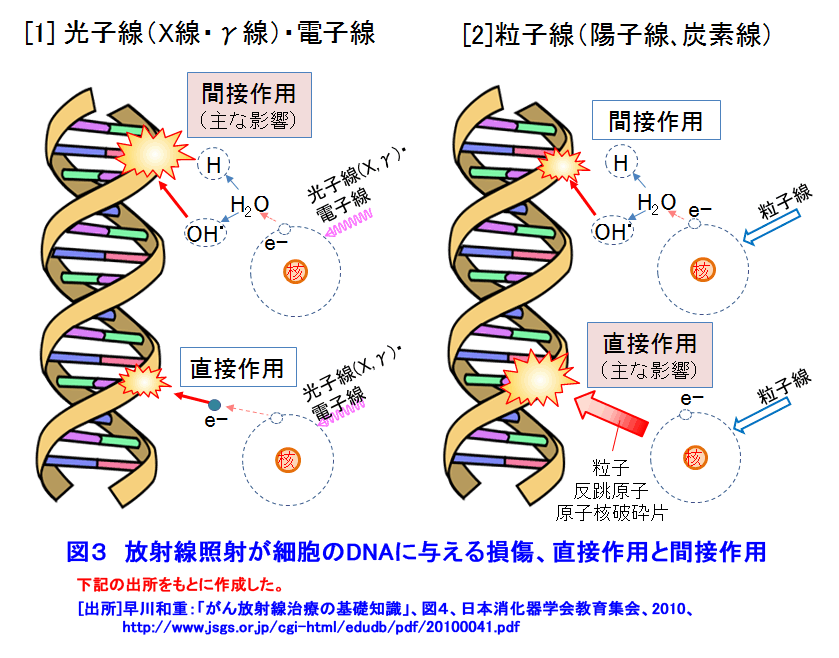
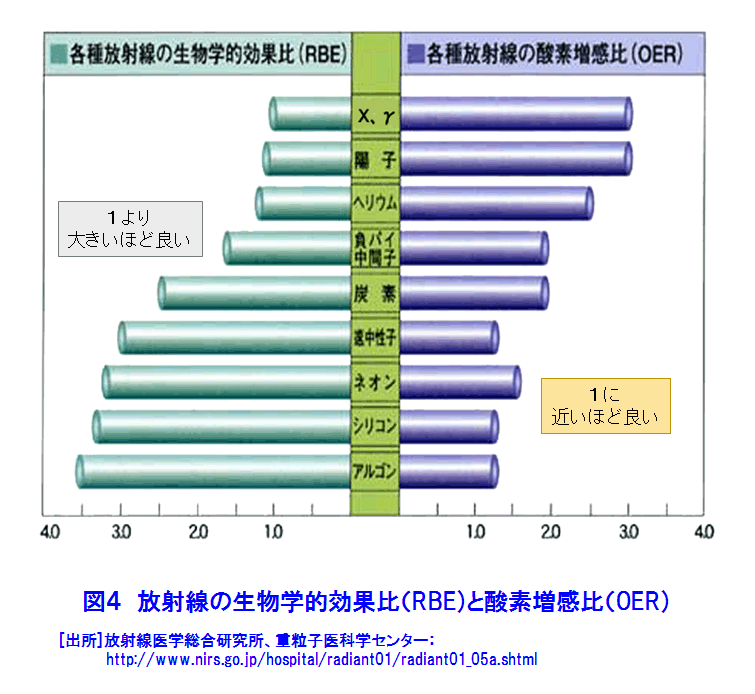
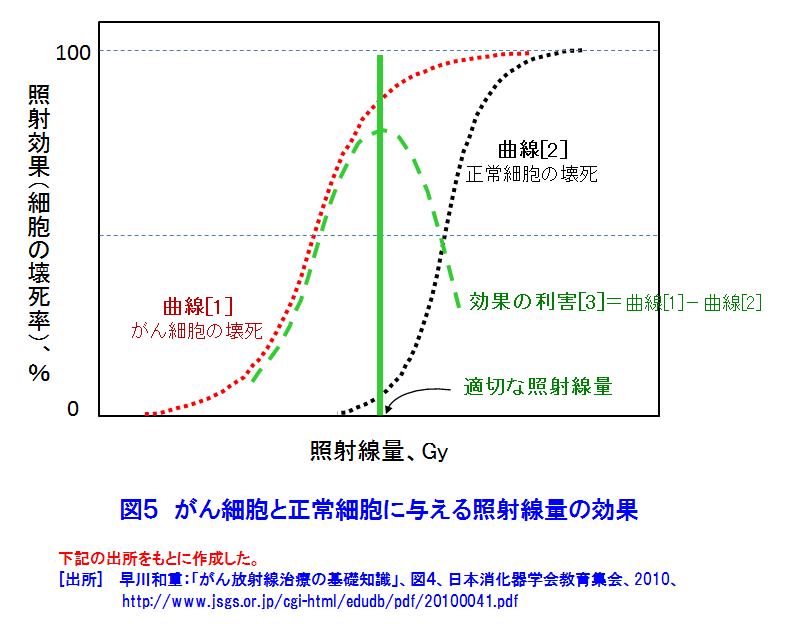
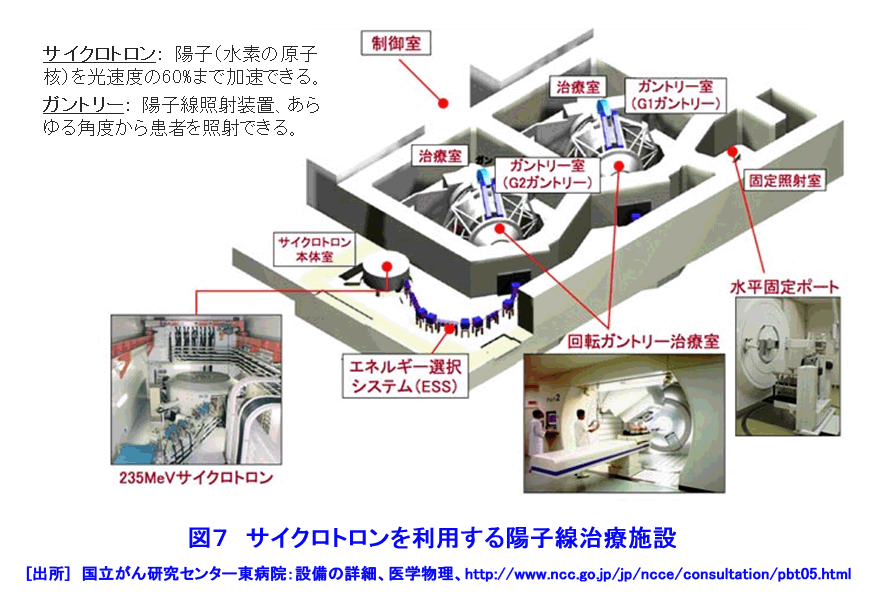
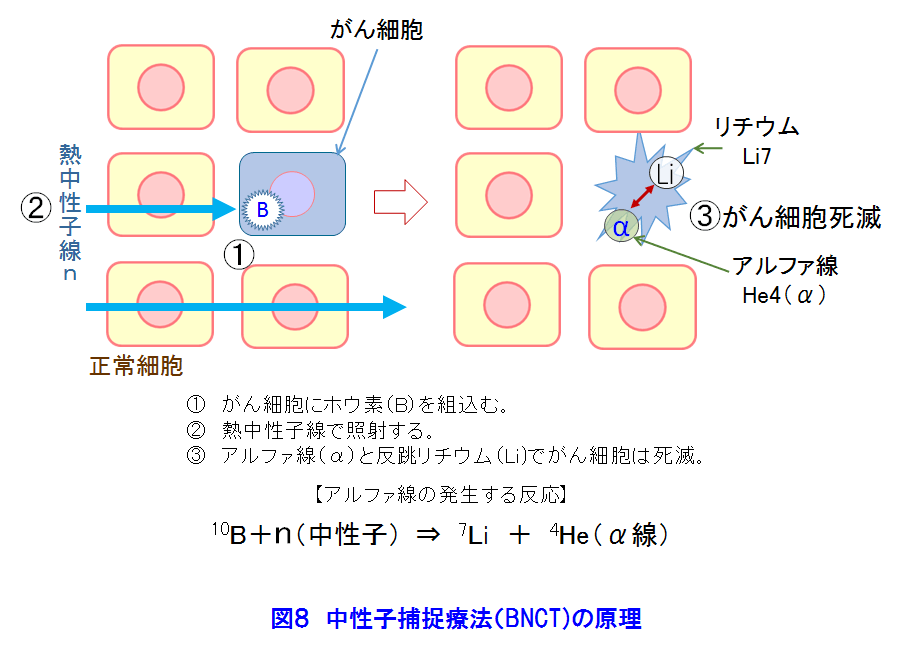
1.がん対策 1.1 日本人の健康とがん対策 がん(悪性新生物)による死亡の割合は、1981年から日本の死亡原因の第1位になり、1984年からがん対策の研究開発と共に質の高いがん医療の普及が進められている。2012年に見直された「がん対策推進基本計画」では、がん予防、がん医療等の普及と共に、重点的に取組む課題に放射線療法、化学療法及び手術療法の充実と医療従事者の育成等を挙げ、あわせて「がんの先進医療技術」の開発推進が図られた。 1.2 がんの放射線治療の歴史 1895年、レントゲンがX線を発見し、翌年には乳がん治療(独)、舌がんと胃がん治療(仏)が試みられた。粒子線利用のがん治療研究は、1955年に米国ローレンス・バークレー国立研究所(LBNL)で始まった。1973年、英国のハウンズフィールドはX線CTを開発し、がん治療に大きな進歩が生まれる契機となった。 日本では、1901年に慣用X線によるがん治療の検討が始まり、1960年に九州大学でベータトロンのX線を利用した治療が開始された。1979年に放射線医学総合研究所が陽子線治療の臨床研究を開始し、1994年に重粒子線(炭素線)治療の研究開発を開始した。 2.放射線治療の特徴 2.1 放射線治療の原理と特徴 (1)がん治療法の分類 図1は、放射線治療を重点に主ながん治療法を示す。放射線治療は、光子線(X線、γ線)と粒子線(電子線、陽子線、重粒子線、中性子線)を利用し、放射線の透過作用、電離作用等による生物学的影響(直接作用と間接作用)でがん細胞を壊死させる。 (2)放射線の透過作用と到達深さ 図2は、身体が放射線照射された際の照射面からの深さと、身体内での放射線の相対吸収線量の関係を示す。光子線(X線、γ線)や電子線は、表面近くで吸収されることから(ビルドアップ)、照射面近くのがん治療に適することが判る。一方、陽子線や重粒子線は、照射面から深い所で相対吸収線量は急に高くなる(ブラッグピーク)。このピークをがんに合わせると、身体深部にあるがん治療に有効であり、がん前後の身体組織の被ばくを低減できる。 (3)放射線の直接作用と間接作用でがん細胞は壊死 身体に吸収された放射線は、身体細胞のDNAに直接作用と間接作用で損傷を与え、DNAの二重鎖切断をひき起こすことなどによりがん細胞を壊死させる。図3[1]に示す光子線による直接作用では、高エネルギーの電離電子がDNAを損壊する。間接作用では電離電子が身体内の水を電離して生じた有害なラジカル(OH-)がDNAを損壊する。間接作用の割合は直接作用より高い。 図3[2]は、粒子線がDNAに与える影響を示す。高LED(線エネルギー付与)の粒子線は高い電離密度の直接作用でDNAを損傷する。この電離作用は、粒子線自体、反跳原子、原子核破砕片等が起こす。直接作用の割合は間接作用より高い。直接作用の細胞周期依存性は小さいので、光子線や電子線に抵抗性のある腫瘍・ガン治療にも治療効果が期待できる。 (4)放射線の生物学的効果(RBE:Relative Biological Effectiveness)と酸素増感比(OER:Oxygen Enhancement Ratio) 図4は、各種放射線のRBEとOERを示す。RBEは、光子線(X線、γ線)を基準にして、放射線が身体細胞に与える影響を示す。RBEが大きい放射線は、がん細胞を壊死させる力が大きい。OERは、放射線の間接作用の一つである酸素効果(放射線の生体への作用は高酸素下ほど大きい)の大きさを示す指標であり、放射線が無酸素状態の身体細胞に与える影響が基準である。OERが大きいと、細胞内の酸素圧に伴い放射線の影響は大きくなる。従って、照射線量(吸収線量)は身体状態に依存する。照射治療には、大きなRBEが望ましい。 (5)分割照射でがんの根治 がん細胞は、分裂頻度が高く正常細胞より増殖するが未分化なので正常細胞より放射線に弱い。また、がん細胞は正常細胞より回復力に劣ることが知られている。図5は、照射線量と細胞の照射効果の関係を模式的に示す。曲線[1]と[2]は、がん細胞は正常細胞より放射線に弱いことを示す。したがって、照射効果の利害曲線[3]から、治療の限界最適線量が示される。最適線量で適切な回復時間を設定した多分割照射によりがんの根治が可能になる。また、分割照射の間には、がんが縮小して酸素が供給され、がん細胞の再酸素化が起き、大きな酸素増感比(OER)の光子線等の照射によるがん細胞の死滅割合が高くなる。 2.2 放射線治療法の利点と技術 上述の原理と特徴から、放射線治療には以下の利点がある:[1]根治治療から緩和治療までの病期全般にわたり利用できる、[2]手術しないので体力の消耗を低減、治療時間は短い、患者の年齢制限は無い、[3]対象器官の形態と機能を維持できて生活の質的低下は小さい、[4]コンピュータと画像診断技術の進歩により、照射治療技術の進歩は目覚ましい。 3.外部放射線治療法−光子線(X線、γ線)と電子線の利用 3.1 光子線の利用 光子線は臨床例が多く放射線治療の主流である。放射線源には、施設・管理コストで優位性がある医療用の線形加速器(ライナック: Linac、リニアックLiniacとも言う)が最も普及しており、2010年には752機関の931台から2014年には824機関の1,066台に増加している。一方、RI(60Co、137Csなど)のγ線利用装置数は、2010年の85台から2014年には63台に漸減している(表1)。 ライナックは、約0.3〜1.3mの電子加速管と標的金属を備えており、電子線とX線を利用できる装置もある。図6は医療用ライナックの例を示す。X線を正常組織の被ばくを避けてがんに正確・効率的に照射するために、三次元原体放射線療法(3D−CRT)、強度変調放射線療法(IMRT)、画像誘導放射線療法(IGRT)、定位放射線療法(STI)、サイバーナイフ(Cyber Knife、放射線治療ロボット)等の新しい照射技術が開発されてきた。IMRTは、がん細胞(組織)と正常細胞(組織)を識別して照射する技術であり、今日では標準的治療法である。 3.2 定位放射線治療装置、ガンマナイフとライナックナイフ コバルト60の密封小線源脳を利用し、脳腫瘍の治療に開発された定位放射線治療装置である。がんの周囲に置いた約200個のCo−60密封小線源のγ線が、がんに集中照射される。放射線がナイフで病巣を切るように照射されるので、ガンマナイフとも呼ばれている。ライナックのX線を利用するライナックナイフも開発されている。 3.3 電子線の利用 電子線は、ライナックから得られ、エネルギーは4MeV〜20MeVである。その身体への透過力はX線やγ線より小さく、体表面や比較的浅いがんや腫瘍の治療に利用される。 4.外部放射線療法−粒子線の利用 光子線や電子線では難治のがん治療が目的にブラッグピークを利用してがんを照射治療する。 4.1 陽子線 陽子線治療は、2001年から10機関が臨床研究を進める「先進医療」技術である(表2[1])。シンクロトロンやサイクロトロンで水素イオンを加速して陽子線を得る。がん周辺の正常細胞への影響を低減出来ることも特徴の一つである。図7は、サイクロトロンによる陽子線治療施設の例である。 4.2 重粒子線 日本での重粒子線は炭素線である。重粒子線は、光子線や陽子線では難治のがん治療が目的である。2003年から4機関が臨床研究を進める「先進医療」技術である(表2[2])。ライナックとシンクロトロンを利用する小型装置の設計が進んでいる。 4.3 中性子線 (1) 速中性子線治療:速中性子線は、光子線に比べ高いがん治療効果が期待され、唾液線、骨・軟部組織等のがん治療に有効性が認められた。しかし、速中性子線はがん細胞と正常細胞へ影響の差異が小さい等の理由から終了した。 (2) 中性子捕捉療法(BNCT):加速器や原子炉で発生する熱中性子を利用し、核反応(中性子n+10B→7Li+4He)を利用して、がん細胞のみを選択的に壊死させる治療法である(図8)。原子炉に代わり、加速器を陽子加速器を利用する中性子源開発が進められている。未だ装置開発と臨床の段階であるが、頭頸部をはじめとする多くのがん治療に効果が期待されている。 5.内部放射線治療法—密封小線源の利用 表3は、主な医療装置への放射性同位体(RI)の供給量を示す。 5.1 密封小線源(図1参照) 密封小線源は、直径約1mm以下のピン状、ワイヤー状やシード状の小さいカプセルに密封された照射用RIである。これら小線源は、がんの近傍の体腔内やがん組織に近接挿入され、身体の中からがんをγ線照射する。 5.2 腔内照射、組織内照射及び表面照射 RALS(Remote After loading System、高線量率小線源治療装置)を利用し、体内に予め挿入したアプリケータ(導管)に沿って密封線源を挿入しがんを照射する。体腔内にアプリケータ挿入する方法は腔内照射といい、腫瘍等に刺しこむ方法は組織内照射という。レジンの型に線源を埋め込み、病巣部に密着させる表面照射は口腔がん等に利用されている。 5.3 非密封線源(図1参照) 日本では、ベータ(β)線を放出する三種類のRIを組込まれた薬剤が利用されている。治療には、これらRI薬剤は、服用または注射で体内に摂りこまれ、薬剤とRIの性質に依って目的のがん組織に集積し放射線照射する。身体内のβ線の飛程は数mmである。甲状腺がんの治療、がんの骨転移の治療等に利用されている。 <図/表> 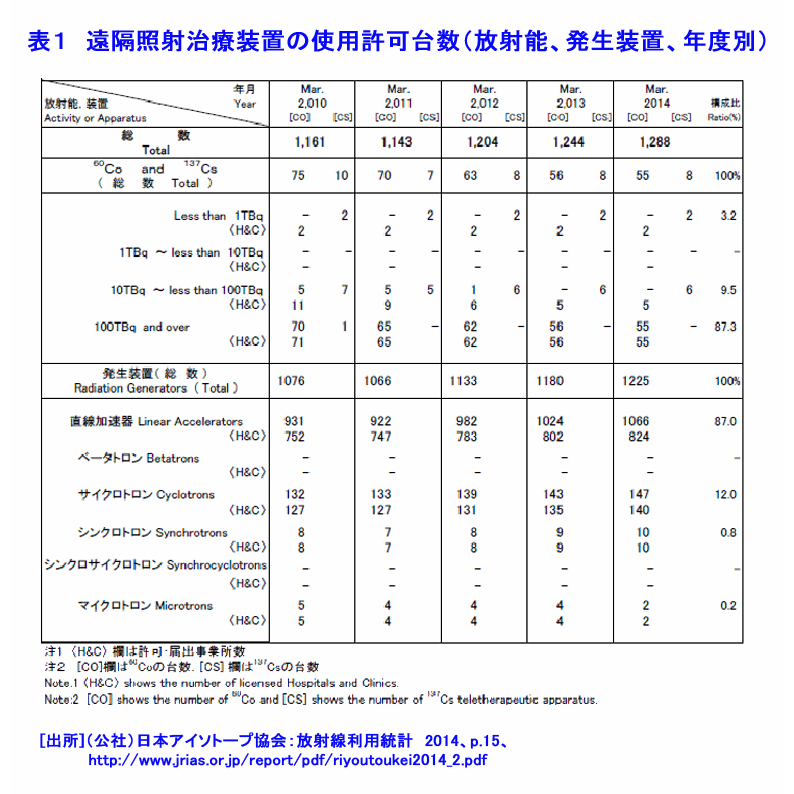


<関連タイトル> 重粒子線照射によるがんの治療 (08-02-02-01) 放射線によるがんの治療(特徴と利点) (08-02-02-03) RI小線源によるがん治療 (08-02-02-04) 中性子を用いたがんの治療(中性子捕捉療法) (08-02-02-05) 高エネルギー加速器の医学での利用(陽子線によるがん治療) (08-02-02-06) 放射線のDNAへの影響 (09-02-02-06) 放射線の細胞への影響 (09-02-02-07) 放射線の直接作用と間接作用 (09-02-02-10) 治療用医療放射線と人体影響 (09-03-04-02) 放射線防護薬剤 (09-03-05-03) <参考文献> (1)(公財)医用原子力技術研究振興財団:切らずに治す粒子線治療 (2)(独)国立病院機構:放射線治療、http://www.ntmc.go.jp/p_sect/contents/46.html (3)尾内能夫:「放射線治療の歴史−わが国における物理・技術を中心にして」、日本放射線腫瘍学会誌、J. Jpn.Soc.Ther.Radiol.Oncol.5, 229−244,1993,https://www.jstage.jst.go.jp/article/jastro1989/5/4/5_4_229/_pdf (4)(国研)国立がん研究センターがん対策情報センター:放射線療法総論、http://ganjoho.jp/public/dia_tre/treatment/radiotherapy/radiotherapy.html (5)(公社)日本放射線腫瘍学会:放射線治療Q&A、http://www.jastro.or.jp/customer/ (6)(国研)放射線医学総合研究所:重粒子線の医学利用 (7)永宮正治:物理学と医学の融合シンポ(東京大学)、加速器と医療(2008)、http://k2.sci.u-toyama.ac.jp/career/event/080314/080314-NAGAMIYA-final.pdf (8)松岡祥介、辻井博彦:(一財)放射線利用振興協会、放射線利用技術データベース、「がん治療に用いられる速中性子線」、http://www.rada.or.jp/database/home4/normal/ht-docs/member/synopsis/040030.html (9)早川和重:「がん放射線治療の基礎知識」、日本消化器学会教育集会、2010、http://www.jsgs.or.jp/cgi-html/edudb/pdf/20100041.pdf (10)放射線医学総合研究所重粒子医科学センター病院:重粒子線治療について知りたい方へ (11)国立がん研究センター東病院:設備の詳細、医学物理、http://www.ncc.go.jp/jp/ncce/consultation/pbt05.html (12)(公社)日本アイソトープ協会:放射線利用統計2014、http://www.jrias.or.jp/report/pdf/riyoutoukei2014_2.pdf (13)厚生労働省:先進医療を実施している医療機関の一覧、http://www.mhlw.go.jp/topics/bukyoku/isei/sensiniryo/kikan02.html
|

