|
<解説記事ダウンロード>
<概要>
ホウ素中性子捕捉療法(Boron Neutron Capture Therapy:BNCT)は、熱中性子とホウ素(10B)の核反応によって放出される極短飛程のアルファ粒子と7Li反跳核によってがん細胞を破壊する治療法である。これにはホウ素化合物が腫瘍に選択的に蓄積(細胞への取り込み、あるいはがん組織での滞留)しなければならない。粒子の殺細胞効果は非常に大きいので強い抗腫瘍効果が認められている。現在、京都大学原子炉実験所及び(独)日本原子力研究開発機構の研究炉の中性子を用いて研究が行われており、悪性脳腫瘍、頭頸部がん、悪性黒色腫(皮膚がんの一種)では有効性が確認されている。更に肝臓がん、肺がんへの応用研究が進んでいる。 <更新年月> 2013年02月
<本文>
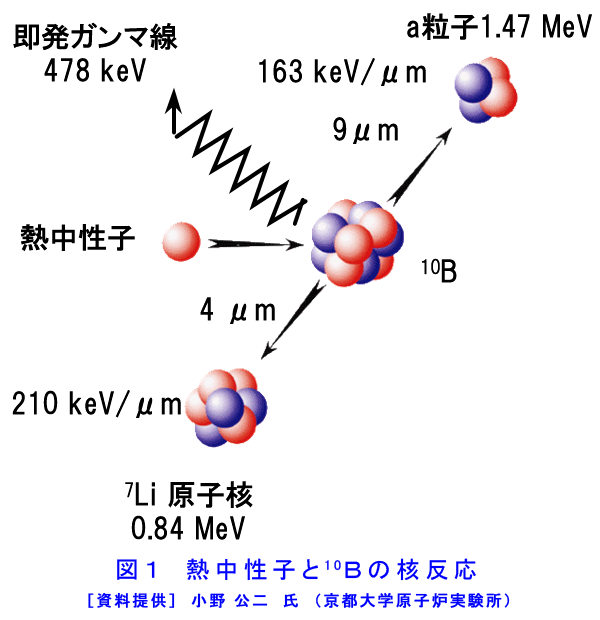
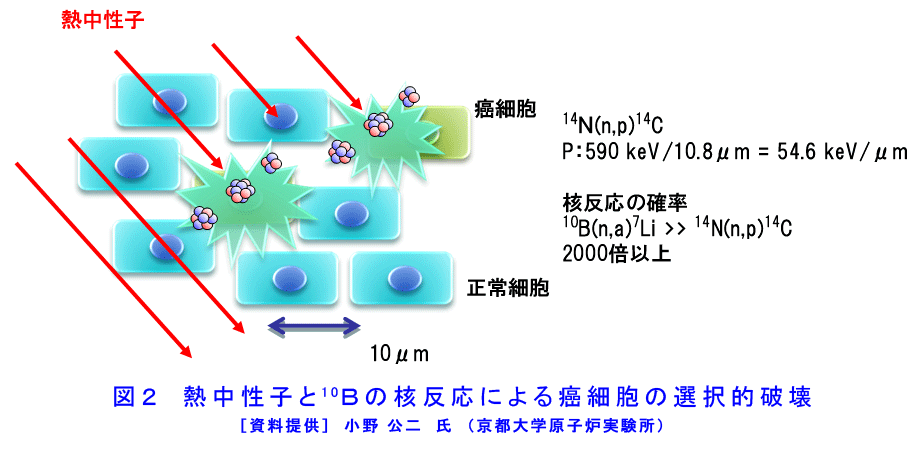
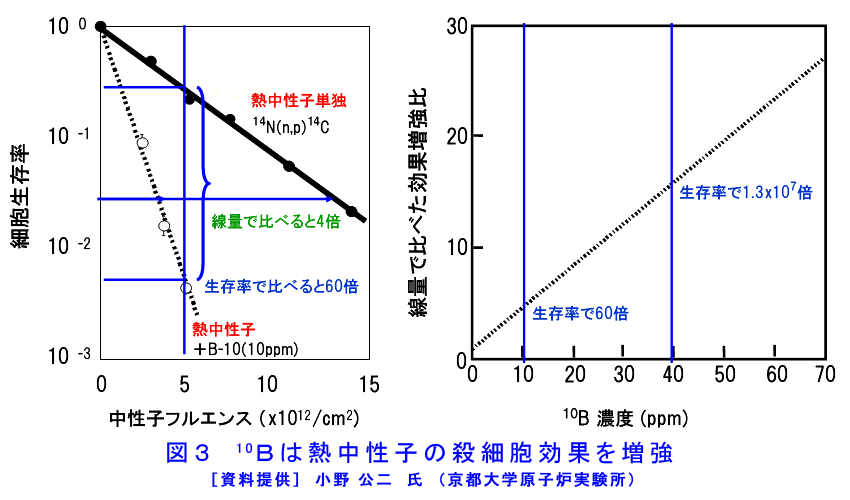
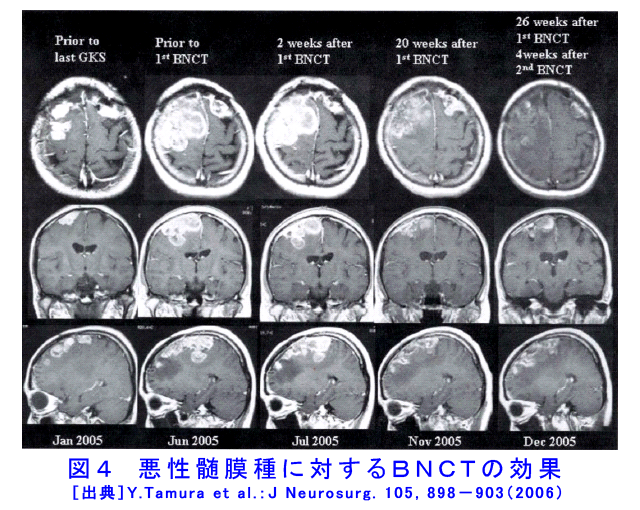
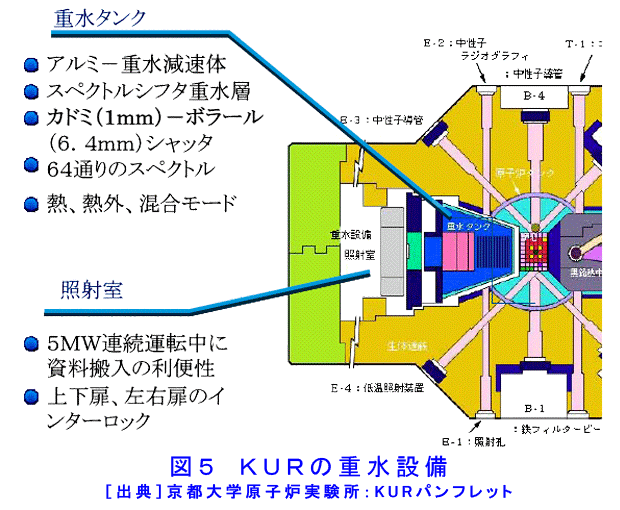
1.BNCTの原理 正常細胞や組織と比べてがん細胞あるいはがん組織に蓄積し易いホウ素化合物をあらかじめ患者に投与し、ホウ素化合物ががんに蓄積した時点で、低速中性子(熱中性子、熱外中性子)を照射すると、中性子とホウ素原子核との核反応(10B(n,α)7Li)によってアルファ粒子とリチウム原子核7Liが放出される。これらの粒子は飛ぶ距離(飛程)が極短い(<10μm)ので、この反応ががん細胞内あるいはその極近傍で起きると、粒子の持つ全ての運動エネルギーがそのがん細胞にのみ与えられ、修復不能なDNAの2重鎖切断が生じて細胞は死滅する。この中性子と10B原子核の反応の確率は、生体構成元素の内最も大きい14N(窒素)と中性子の反応確率の2000倍以上である。従って、ホウ素化合物ががんに選択的に蓄積すれば、そこへ低速中性子を照射することによってがんを選択的に破壊できる(図1、図2及び図3を参照)。この治療の成立には、ホウ素化合物が選択的に集積するがんであることが前提となるが、高い選択性と強力な殺細胞効果のため、通常のX線には抵抗性でかつ広範囲に浸潤するがん、X線治療後の再発がん、同一臓器に多発の病巣を有するがん、極めて形状の複雑ながん等が適応になる。悪性脳腫瘍、悪性黒色腫、再発頭頸部がん、多発肝がん、肺がん等である。 2.歴史と現状 BNCTは、1936年に米国のG.L.Locherによりその可能性が提唱され、その後幾人かの研究者によって動物実験でその効果が確認された。実際の臨床試験が行われたのは1950年代に米国ブルックヘブン国立研究所(BNL)の医療用原子炉(BMRR)が完成してからであり、1950年代にこの原子炉を用いて脳腫瘍の治療が盛んに試みられた。しかし、用いられたホウ素化合物(硼砂、または5ホウ酸ナトリウム)が、がん組織に選択的かつ十分には蓄積しなかったこと、及び中性子線の質にも不十分さが在り、目的とする腫瘍の選択的な照射ができなかったことが主な理由となって、期待した効果が得られないままに中止された。その後しばらく米国での照射例は報告されていなかったものの、1984年には国際中性子捕捉療法学会が設立され、また、わが国での研究の進展(後述)に刺激され1994年にBMRRを用いての臨床試験が再開された。マサチューセッツ工科大学(MIT)のMITR-IIでも悪性黒色腫(皮膚がん)の臨床試験が行われた。ヨーロッパではオランダ・ペッテンにあるHFR、スウェーデンのスツービック(Studvik)の研究炉、フィンランドの研究炉エスポーなどで主に脳腫瘍を対象に試験研究が行われた。しかし、夫々、研究体制の脆弱さやわが国とは異なった研究文化のため十分な成果を生まないまま、完全撤退(米国BNLのBMRR、スウェーデンのスツービック原子炉)あるいは休止(米国のMITR-II、オランダのHFR)の状態にあり、現在も活発に研究が継続しているのはフィンランドの研究炉(FiR-1)においてのみである。 一方、日本においては故畠中坦教授が、米国から持ち帰った化合物の中から最も脳腫瘍への蓄積(化合物の滞留)に優れたホウ素化合物(Na2B12H11SH:BSH)を選び出し、これを用いて精力的な臨床試験研究を実施した。わが国における最初の医療照射は1968年HTR(日立炉)で行われた。試験研究の結果は、通常の手術+X線治療と同等か、それ以上の効果と評価され、次第に認められるようになった。ただ、組織への深達性に乏しい熱中性子の故に、中性子照射に際して原子炉サイトでの開頭手術が必要であり、これが研究発展の大きな制約因子の一つになっていた。こうした状況を一変させ、また適応拡大に路を開く契機となったのは、1987年、三嶋豊教授(神戸大学)の行ったパラボロノフェニルアラニン(BPA)を用いた世界最初の悪性黒色腫のBNCTであった。BPAは能動的にがん細胞が取り込むホウ素化合物で、その選択性も高い。BPAを得て、BNCTは初めてがん細胞選択的と言う看板に相応しい治療になった。その後、BPAが集積するがんの探索が18F - BPA PETを用いて上田聖教授、今堀良夫講師(共に京都府立医科大学)によって先駆的に行われ、BPAは悪性黒色腫に限らず、多くの腫瘍で良好な選択的集積性を示すことが分かった。この結果を踏まえて、上田・今堀と小野公二教授(京大原子炉実験所)らのグループは、BPAを用いた悪性脳腫瘍のBNCTを1994年2月に世界で最初に実施した(F-BPA PET-BNCTシステムの確立)。中性子照射に際して開頭術を必要としない熱外中性子の利用で、わが国は米国や欧州の後塵を拝していたが、1996年の京大炉(KUR)の重水設備改修によって、また、遅れて、(独)日本原子力研究開発機構の4号炉(JRR-4)において熱外中性子ビームの利用が可能となり、深部の腫瘍治療にも適用させ、世界のトップレベルの照射条件を有している。その結果、故畠中教授の後継の人たちがその手法を踏襲して行っていた脳腫瘍の術中BNCTは、現在では略過去のものとなっている。BNCT研究での次の大きな飛躍は2001年末、KURで小野教授のグループと加藤逸郎歯科医師(阪大・歯)が共同で行った再発耳下腺がんに対するBNCTであり、そこで示された選択的抗がん効果は、わが国は言うに及ばず米国、欧州のBNCT研究に大きなインパクトを与えた。現在では欧州でも再発頭頸部がんを対象としたBNCT臨床試験研究が開始されている。更に頭頸部がんのBNCTでは、腫瘍栄養動脈からの超選択的ホウ素化合物投与の試みが、小野教授と不破信和(愛知県がんセンター・放治・部長)との共同によって行われ、その優れた効果が確認された。現在、頭頸部がんのBNCT研究はKURグループと平塚純一(川崎医大・放・准教授)・粟飯原輝人(同・耳鼻・講師)及び加藤歯科医師の共同研究によって強力に推進されている。悪性脳腫瘍のBNCTは2002年から、非開頭照射となり、BSHとBPAの2剤併用、中性子深部分布の改善を目指した術後死腔への空気充填、照射野の中央部遮蔽などの実に多くの試みが小野教授グループと宮武伸一(大阪医大・脳・准教授)・川端信司(大阪医大・脳)らとの共同で進められ、最近の治療成績では膠芽腫の2年生存率で50%、生存中央月数で24か月を超えるに至っている。また、悪性髄膜腫に対するBNCTの先駆的試みも実施され、その優れた効果が確認されている(図4)。現在、わが国の悪性脳腫瘍BNCT症例の殆どはこのグループによって実施されている。また、最近では、多発肝がんや肺がん(中皮腫を含む)に対するBNCTの先駆的試みが小野・鈴木実(京大・原子炉実験所)によって実施され、効果が確認された。 こうした臨床研究の進展を支えたのは、工学、医学物理学研究である。治療計画の立案に不可欠な線量計算や照射シミュレーションシステムの開発が行われ、熊田博明(日本原子力研究開発機構・研究員)の努力によってBNCT線量評価システム((独)日本原子力研究開発機構 Computational Dosimetry System:JCDS)の完成を見た。さらに、肝がん照射などでの正常組織線量を照射中に常時把握するための遠隔線量モニターシステムが櫻井良典・丸橋晃教授(京大・原子炉実験所)によって開発、設置された。 また、(独)日本原子力研究開発機構ではJRR-4におけるBNCTの確立に資するための技術開発を行っている。より高度な照射が期待されるなか、異なる二つのホウ素化合物(BPA、BSH)の濃度測定の困難性、患者の位置変動の生じ易さなどにより、照射精度に影響を与える因子も多く、これらを踏まえ、照射技術の高度化、線量評価技術の高度化、ホウ素濃度測定技術の開発等を行っている。 KURを用いたBNCTの累積件数は、2010年(平成22年)12月末の時点で306件に達した(燃料低濃縮化のため、2006年4月から2010年4月まで一時休止)。また、JRR-4では1999年(平成11年)10月25日から107例(2012年7月時点)の医療照射が実施されている。このように、現在、わが国のBNCT研究は量、質、共に世界の研究を牽引する位置にある。 (注:文中、各氏の所属機関は当時のものである。) 3.BNCTのための中性子源 BNCTでは中性子フルエンス率の大きい中性子源が必要である。そのため、利用できるものは、現状では研究炉以外に無く、今日までに使われてきた原子炉は主として武蔵工業大学のMITRR、京都大学のKUR及び(独)日本原子力研究開発機構のJRR-2、JRR-4である。その内、現在も利用可能なものはKURとJRR-4の二つである。両者の熱外中性子ビームを比較すると(表1参照)、KURの熱外中性子ビームには熱中性子の混入が皆無であるに対し、JRR-4のそれには混入がある。これらは、医療照射に当たって皮膚線量の差に有意な影響を与えている。また、γ線の混入もJRR-4の方が大きい。JRR-4の優れた点は中性子強度がKURのそれに数倍していることであり、照射時間を短縮できる大きなメリットがある。さらにビームの中心と床面との距離が大きく、患者の体位設定が容易である。現在、JRR-4でBNCT研究を実施している大学などは、筑波大学、香川小児病院、京都大学、川崎医科大学、大阪医科大学、徳島大学、大阪大学、東京大学である。KURはビームシャッターを装備しており、原子炉の連続運転下に患者の出し入れが可能であるので、一日に照射できる数が多い。この点は、何れの炉も医療専用炉でないことを考えると、優れた点と言える。両原子炉の医療照射設備の概要図を図5(KUR)及び図6(JRR-4)に示す。現状の多目的炉を使う限り、医療利用における不便は解消し得ないので、医療専用炉建設の希望が医療側から出され、一部企業で検討されたが本格的には進展しなかった。それは、原子炉の立地の制約、特有の規制から解き放たれない限り、真の医療としての確立は無いとの考えによる。現在では原子炉に代わって加速器中性子源開発を進める流れにあり、わが国でも複数のプロジェクトが立ち上がっている。 その一つとして、茨城県における、県内にある世界最高レベルの高度な技術や研究成果を活用し、最先端のがん治療であるBNCTの実用化を推進するため、産学官連携による実証的な共同研究を行う「いばらき中性子最先端医療研究センター」の整備がある。筑波大学、高エネルギー加速器研究機構、日本原子力研究開発機構のほか企業を含めて、病院で安全確実に治療が行える世界初の小型加速器によるBNCT治療装置の実用化を目指すこととしている。 各々の原子炉での医療照射(BNCT)の実績などは、京都大学原子炉実験所及び(独)日本原子力研究開発機構のHPから見ることが出来る。 <図/表> 

<関連タイトル> JRR-4 (03-04-02-03) 核医学診療分野における脳機能の解明 (08-02-01-06) 放射線によるがんの治療(特徴と利点) (08-02-02-03) JRR−4におけるホウ素中性子捕捉療法(BNCT) (08-02-02-17) <参考文献> (1)舘野之男:放射線医学史、岩波書店(1973) (2)Y.Mishima et al.:Lancet Aug 12:2(8659),388-389(1989) (3)畠中坦:Boron Neutron Capture Therapy for Tumours、西村書店(1990) (4)K.Ono et al.:Int. J. Radiat. Oncol. Biol. Phys. 34(5),1081-1086(1996) (5)K.Ono et al.:Int. J. Radiat. Oncol. Biol. Phys. 43(2),431-436(1999) (6)S.Imahori et al.:J. Nucl. Med. 39,325-333(1998) (7)日本原子力研究所研究炉部(編):研究炉利用ハンドブック 改訂第2版(1999年3月) (8)S.Kawabata et al.:J Neuro-Oncol. 65(2),159-65(2003) (9)S.Miyatake et al.:Journal of Neurosurgery,103(6),1000-1009(2005) (10)I.Kato et al.:Applied Radiatyion and Isotpoes,61,1069-1073(2004) (11)M.Suzuki et al.:Jpn. J. Cancer Res. 91(10),1058-1064(2000) (12)M.Suzuki et al.:Int. J. Radiat. Oncol. Biol. Phys. 58(3),892-896(2004) (13)M.Suzuki et al.:Int. J. Radiat. Oncol. Biol. Phys. 59(1),260-266(2004) (14)Y.Sakurai et al.:Applied Radiation and Isotopes 61,829-833(2004) (15)M.Suzuki et al.:Int. J. Radiat. Oncol. Biol. Phys. 66(5),1523-1527(2006) (16)M.Suzuki et al.:Int. J. Radiat. Oncol. Biol. Phys. 66(5),1584-1589(2006) (17)小野公二、他:ホウ素中性子捕獲療法(BNCT)の現状と将来の展開、Isotope News,No.631,2-6(2006年11月) (18)T.Aihara et al.:Head & Neck 28,850-855(2006) (19)Y.Tamura et al.:J Neurosurg. 105,898-903(2006) (20)Y.Sakurai et al.:Phys.Med.Biol. 51,1-11(2006) (21)京都大学原子炉実験所:KURパンフレット (22)(独)日本原子力研究開発機構:17年度(2006年)研究炉加速器管理部年報 (23)(独)日本原子力研究開発機構 JRR-4:http://jrr4.jaea.go.jp/3/31.htm (24)京都大学原子炉実験所:ホームページ、http://www.rri.kyoto-u.ac.jp/BNCT/bnct.html
|

