|
<解説記事ダウンロード>
<概要>
放射線ホルミシスとは、高線量では有害な放射線が低線量では生物活性を刺激する、あるいは“適応応答”と呼ぶ後続の高線量照射に対する抵抗性を誘導するなどの現象をいう。近年、分子、細胞レベルから個体レベルまでの多様な放射線ホルミシス現象が見出され、研究が進められている。電力中央研究所の最近(2003年)の研究成果にもふれる。 <更新年月> 2004年08月
<本文>
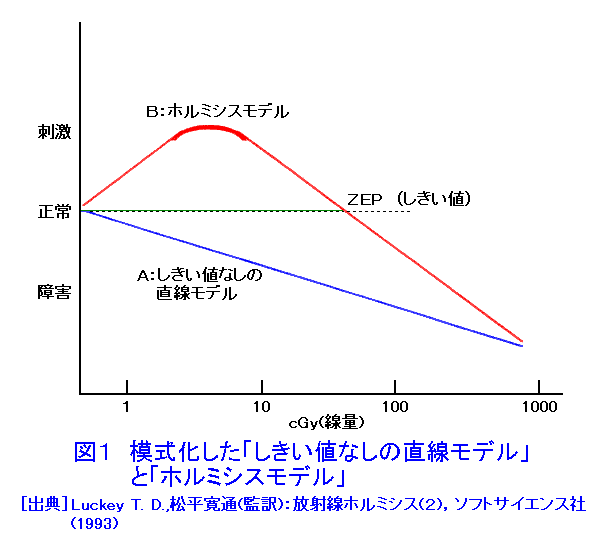
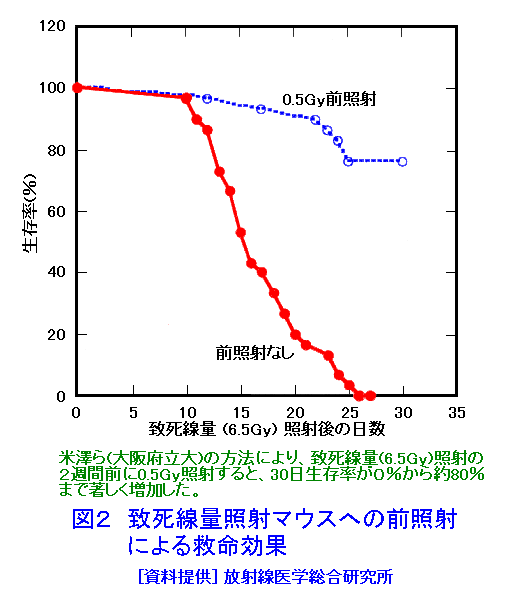
1.はじめに 高線量の放射線は、急性放射線障害や発がんなどの障害を引き起こす。従来、放射線生物影響に関する研究は、“放射線はすべて、どんな低い線量でも生物に対して障害作用をもつ”との“常識”に沿って行われてきた。ところが、膨大な障害研究の中に埋れていたデータの見直しなどから、1980年代に入って、低線量の放射線はかえって有益な効果があるとの主張がなされるようになり(文献1,2)、これまでの“常識=パラダイム”にとらわれない新たな視点からの低線量影響研究が行われ始めた。高線量域での影響から予測できない特異的なホルミシス効果が相次いで報告され、その研究は放射線生物学の中心的な課題の一つとして進められている(文献3−6)。 2.“放射線ホルミシス”と“放射線適応応答”−言葉の定義 ホルミシス(hormesis)という言葉は、ギリシャ語“horme”、すなわち“=to excite”に由来し、ホルモンと同じ語源を持つ。大量では有害作用を有する各種の作用源が、少量では生理機能の刺激効果を有することを指す。 ホルミシスの概念は、図1の模式的な線量−効果(応答)曲線により端的に示すことができる。Aの直線は、どのような量でも生物学的に有害でプラスの効果がなく、有害な効果が量と共に増大するとする、“しきい値なしの直線モデル(LNT仮説)”である。従来の放射線影響研究はこの立場に立っていた。一方、Bの曲線で表されたホルミシスの場合には、少量で極大のプラス効果を持つ刺激が生じる。さらに用量を上げていくと、効果がないゼロ相当点(ZEP:zero equivalent pointの略)に達し、これが“しきい値”であり、その点を境として量が増えるにつれて有害なマイナス効果が増大する。 低線量放射線によって、高線量で起こる障害とは異なる刺激効果が生じることを “放射線ホルミシス”と言う。 刺激あるいはストレス反応性は、生物、細胞の持つ基本的な特性の一つである。刺激が繰り返されると、刺激に抵抗性となる。これを適応応答(adaptive response)と呼ぶ。“放射線適応応答”とは、一般的には低線量の放射線により、後続の高線量照射に対する抵抗性が誘導される現象を指すが、広義には放射線ホルミシスと同義語のように使われる場合もある。 3.放射線ホルミシスおよび適応応答現象 生物は現在より高い自然放射線の環境下で生じ、放射線に限らず多様な物理的、化学的ストレスのある状態の中で進化してきた。ホルミシスは、こうした多様なストレスに対し、生体が進化の過程で獲得してきた重要な生体防御機構と考えられる。 放射線ホルミシス現象は、分子、細胞から個体レベル、さらには疫学データにおよぶ多岐にわたる系で検出されている。細胞増殖の促進、免疫能の亢進、成長促進、寿命延長、疾病抑制、がん発生率や死亡率の低下その他、多様なホルミシス効果が認められている。 低線量放射線のホルミシス効果を示す例として、ゾウリムシを鉛の箱で自然放射線を遮断して飼育すると、正常の増殖能が抑制され、放射線源を入れると回復したという知見もある。 ホルミシスを誘発する低線量として、多くの系で一回の照射の場合は1−20cGyで特異的に認められ、50cGy(センチグレイ)以上ではこうした効果が消失することが多い。また、放射線に限らず、熱、紫外線などの物理的ストレス要因やDNA損傷性物質などでも、同じような生体反応を引き起こすことが観察されている。 低線量前照射により放射線抵抗性を誘導する“適応応答”も、放射線に限らず微量の各種のDNA損傷物質やストレス要因によっても誘導され、また、逆に低線量放射線がそれらの要因に対する交叉適応を誘導する。 放射線適応応答として、細胞レベルでは染色体異常、突然変異、細胞死、免疫系障害などの軽減、動物実験で、免疫系の亢進、発がん、がん転移の抑制、奇形発生や致死の抑制など多くの効果が認められている。図2にわかりやすい例として、致死線量照射マウスに、0.5Gyを2週間前に照射して生じた顕著な救命効果を示した。 4.低線量照射とがん 高線量の放射線は、白血病を始めとするがん死亡率の増加を引き起こす。そこで、放射線発がんリスクに対し、現在、ICRPから出されている勧告値は、図1のAの“しきい値なしの直線モデル(LNT)”に基づいている。しかし、低線量での発がん増加を実際に示すデータはない。 一方、高バックグラウンド地域の住民、職業被ばく者、原爆被ばく者、医療被ばく者などについての低線量影響の疫学調査では、リスク推定からの予想と異なり、むしろ発がん率の低下も報告されている。動物実験でも低線量前照射により、放射線発がんのみならず、化学発がんの抑制や、がん転移の抑制など、発がん、制がんと関連した多くのホルミシス効果が認められている。 さらに、放射線はがん治療の重要な手段であり、一般的に局所照射によりがん細胞を殺すため高線量照射による治療が行われている。ところが、10cGyの低線量全身照射を繰り返すホルミシスに基づく方法で、局所照射治療法より高い治癒率が得られたとの報告もある。 5.放射線ホルミシスの機構 放射線は直接、あるいは照射により生じた活性酸素(ROS)によって、DNA損傷を起こし、これががんの原因となる可能性がある。しかし、こうしたDNA損傷は、生体内で生理的に生成するROSによっても生じ、その数は自然放射線により生じる数よりも桁違いに多いと考えられている。 生体内にはこうしたDNA損傷を抑制し、除去する多段階の機構が備わっている。先ず、活性酸素をSODなどの酵素やグルタチオンなどの物質により除去する。次いで、損傷DNAを分子レベルで修復する複数の修復系が存在し、さらに、残ったDNA損傷をもつ細胞は、免疫系やアポトーシスという細胞死によって除去される。 低線量放射線により、こうした分子レベルから細胞レベルにいたる多様なDNA損傷抑制機構が亢進することが明らかにされている。 低線量放射線照射による多様な遺伝子の発現亢進や、がん抑制遺伝子産物p53やストレスタンパク質などの増加が検出されている。これらの多くは、放射線以外の多くのストレス要因によっても誘導される。こうした遺伝子産物のホルミシス発現への重要性はp53ノックアウトマウスなどの遺伝子改変動物や細胞を用いた研究によっても明らかにされつつある。 さらに、免疫能賦活、細胞周期調節なども放射線ホルミシスに関与していると考えられ研究が行われている。 表1に分子レベルから個体レベルまでのホルミシスの例を示した。 6.日本での研究と世界の動向 低線量の研究は、放射線の生物作用の全体的な理解のために欠かせない重要性を持っている。1980年代から始まったホルミシスの研究に関し、多くの国際学会やシンポジウムが開かれている。国連科学委員会(UNSCEAR)は、1994年報告の付属書「細胞および生物における放射線適応応答」において研究の続行を勧告している。 日本では、1980年代の早くからホルミシス効果についての研究が始められ、多くの大学や研究所で世界に先んじた研究が進んでいる。1987年、日本放射線影響学会において「放射線ホルミシス研究会」が発足した。また、電力中央研究所が中心となり、1988年以来国内外の20余の研究機関が連携した研究プロジェクトも進展している。世界各国でのホルミシスへの関心が急速に高まって、研究が一段と加速している。 電力中央研究所の最近の成果では、(1)自己免疫疾患による糖尿病(I型)のマウスに、0.5Gyの放射線を高線量率(94.2Gy/hr)または低線量率(0.95mGy/hr)でそれぞれ照射したところ、高線量率照射では抗酸化物質の増加や糖尿病発症抑制の効果が認められたり、(2)化学発がん剤を皮下に投与したマウスを3群に分け、それぞれ0.35、1.2および3.5mGy/hrの線量率で照射を216日間続けたところ、1.2mGy/hrで照射したマウスの群において、腫瘍発生率の有意な抑制が見られたという報告がある。 近年、こうしたホルミシス研究の進展に伴って、しきい値なしの直線モデル(LNT)に基づく ICRP勧告値の妥当性についての論争も行われるようになっている。 <図/表> 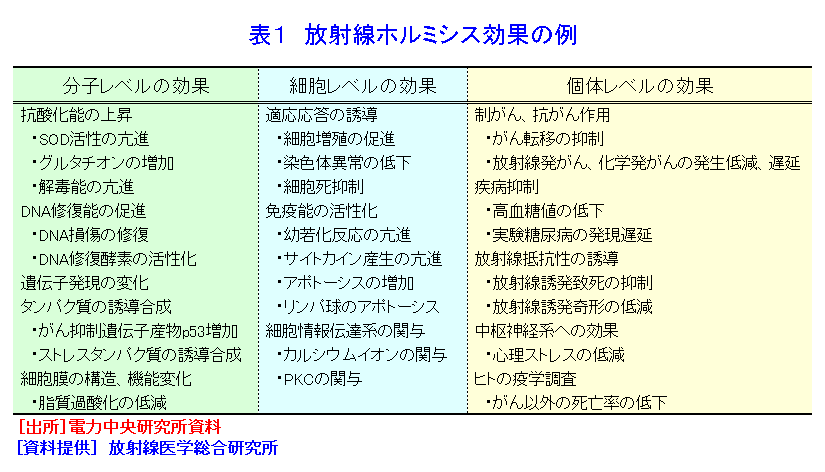
<関連タイトル> 中国の高自然放射線地域における住民の健康調査 (09-02-07-01) <参考文献> (1)Luckey T. D.,松平寛通(監訳):放射線ホルミシス、 ソフトサイエンス社(1990) (2)Luckey T. D.,松平寛通(監訳):放射線ホルミシス(2),ソフトサイエンス社(1993) (3)大山ハルミ、山田武:低線量放射線の健康影響−放射線ホルミシス、RADIOISOTOPES vol.46, p.360−370(1997) (4)国連科学委員会、放射線医学総合研究所(監訳):国連科学委員会(UNSCEAR)1994年報告書、付属書、放射線の線源と影響、「細胞および生物における放射線に対する適応応答」、実業公報社(1996年) (5)Feinendegen,L. E. and Polycove,M.: Biological responses to low doses of ionizing radiation,detriment versus hormesis,Part 1 and 2,J. Nucl. Med. 42,17N-37N,2001 (6)Yamada,T. et al.(eds): Biological Effects of Low Dose Radiation,Elsevier,Amsterdam,2000. (7)電力中央研究所 原子力技術研究所 低線量放射線研究センター:報告書「I型糖尿病モデルマウスの糖尿病発症および抗酸化物質に及ぼす線量率の効果」(2003年) (8)電力中央研究所 原子力技術研究所 低線量放射線研究センター:報告書「マウスにおける低線量率長期照射の発がん抑制効果−メチルコラントレン誘発皮下がん−」(2003年)
|

