|
<解説記事ダウンロード>
<概要>
放射線抵抗性細菌から取得された放射線感受性変異株のゲノムDNAで突然変異を起こしている遺伝子を探索することによって、放射線抵抗性細菌のDNA2本鎖切断修復に重要な役割を果たしている新規遺伝子が同定された。この遺伝子から作られるタンパク質PprAは、放射線などによってDNA鎖が切れた部分を認識して結合することにより、DNA鎖切断の修復を高効率で促進する活性を持つ。PprAタンパク質のDNA修復促進活性を利用し、DNAリガーゼと組み合わせることによって、新しいバイオ研究試薬が開発され、高効率のDNA修復試薬「TA-Blunt Ligation Kit」として発売されている。このDNA修復試薬は、今後、バイオ研究に幅広く用いられ、遺伝子診断や新薬などの開発に役立つことが期待される。 <更新年月> 2006年06月
<本文>
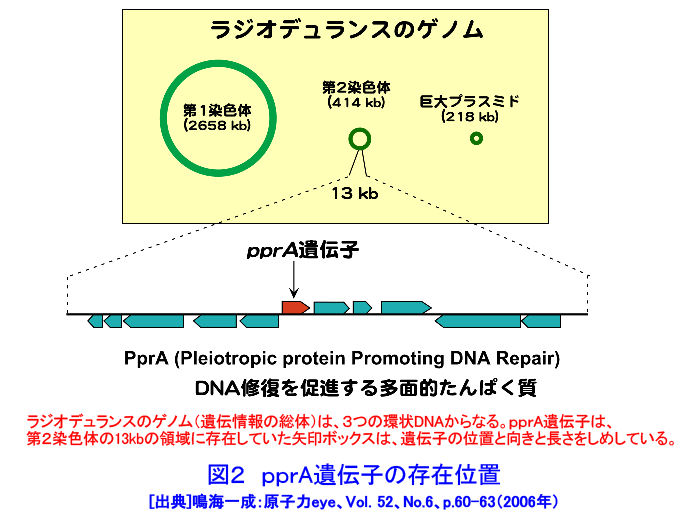
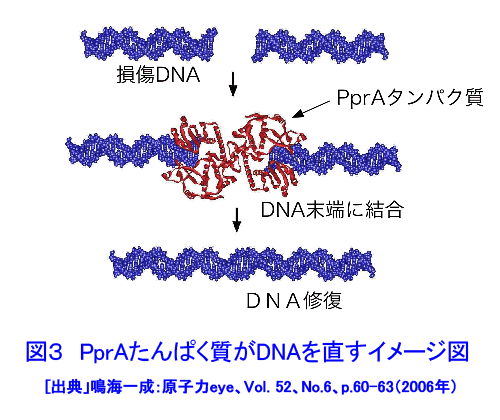
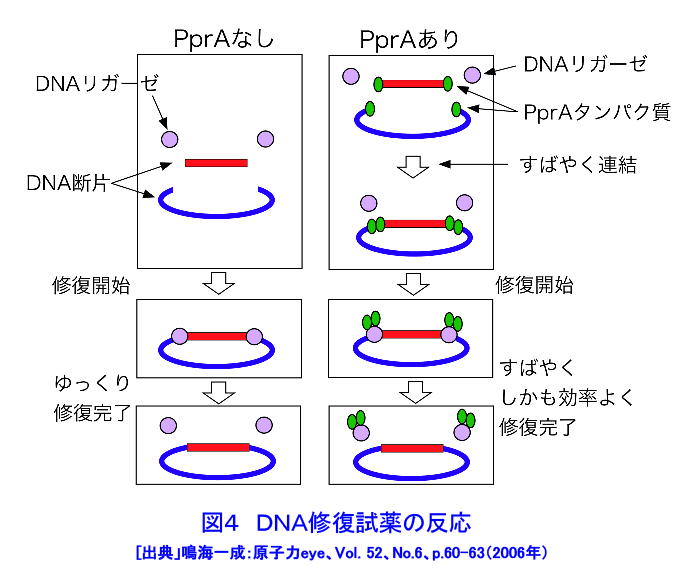
1. 放射線抵抗性細菌のポストゲノム研究 電離放射線による生物効果で最も重篤な障害はDNAの2本鎖切断であり、2本鎖切断に対する修復能力が優れていることが、放射線抵抗性細菌デイノコッカス・ラジオデュランス(Deinococcus radiodurans)(図1)の最大の特徴である。また、放射線抵抗性の優れた細菌の2本鎖切断修復には、放射線照射後に誘導されるなんらかのタンパク質が重要な役割を果たしていることが1960年代には分かっていた。したがって、放射線抵抗性細菌の極めて高いDNA修復能力の原因を突き止めるためには、2本鎖切断修復に係わり、放射線で誘導されるDNA修復タンパク質を同定することが重要であると考えられていた。 この考えのもとに、米国では1995年に米国ゲノム研究所において、D. radioduransのゲノムプロジェクトが開始され、1999年に全ゲノムDNAの塩基配列が決定された。次に、このゲノムDNA配列情報をもとにして、放射線照射による細胞内タンパク質量の変動を解析するために、米国のPacific Northwest 国立研究所がプロテオーム解析(タンパク質発現プロファイルの網羅的解析)を行い、また、放射線照射による遺伝子発現の変動を解析するために、米国Oak Ridge国立研究所ではトランスクリプトーム解析(mRNA発現プロファイルの網羅的解析)が行われた。放射線抵抗性細菌のゲノムプロジェクトで明らかになったのは、放射線抵抗性細菌が3187個の遺伝子を持つこと、並びにそれらのゲノム上での位置関係であった。また、既知の遺伝子との相同性検索によって、全遺伝子の52%が機能未知遺伝子であること、放射線抵抗性細菌は今までに他の生物で知られているDNA修復関連遺伝子のほとんどを持っていることが分かった。しかし、この様な遺伝子は、放射線に弱い大腸菌など一般の他の細菌も持っているので、DNA塩基配列情報の解析からは、結局、放射線抵抗性細菌の著しく高いDNA修復能力の原因が何であるのかを明らかにすることは出来なかった。米国の国立研究所が行ったトランスクリプトーム解析によって、放射線で誘導されると予想されるタンパク質群が50種類ほど同定されたが、プロテオーム解析の結果と一致しないものもあり、放射線抵抗性細菌の2本鎖切断修復に重要な役割を果たしているタンパク質を同定するまでには至らなかった。 2. 新規DNA修復促進遺伝子の発見 D. radioduransのDNA修復機構解明のためのもう1つの研究方法として、D. radioduransに変異原処理をして取得した放射線感受性変異株(遺伝子のどこかに変異が起こったため放射線に弱くなった菌)を解析して,放射線耐性に重要な役割を果たしている遺伝子を同定するという分子遺伝学的方法がある。この方法では、野生株(放射線に耐性を持つ正常な株)から抽出した様々なDNA領域の断片を放射線感受性変異株に導入して、放射線感受性変異株を放射線耐性に復帰させることのできるDNA領域を限定する作業を繰り返し、最終的に放射線感受性変異株の放射線感受性の原因になっている遺伝子を同定することができる。 この方法を用いて、放射線感受性変異株の1つであるKH311株の原因遺伝子が同定された(図2)。国際DNAデータバンクのDNA塩基配列データベースと照合した結果、同定された遺伝子のDNA塩基配列ならびに遺伝子から作られるタンパク質のアミノ酸配列は、データベースに登録されているどの遺伝子の配列とも全く似ておらず、ゲノムプロジェクトで機能未知遺伝子に分類されていたものの1つであった。放射線感受性変異株のこの遺伝子のDNA塩基配列は、野生株と較べて、1箇所のみ異なっていることが分かった。すなわち、放射線感受性変異株では、1つの遺伝子のたった1箇所の変異によって,放射線耐性が失われていたのである。 DNAを修復する際に実際に働くのは、遺伝子から作られるタンパク質である。このタンパク質の性質を生化学的に解析した結果、放射線などによってDNA鎖が切れた部分を認識して結合することによってDNA鎖切断の修復が高効率で促進されることが分かった(図3)。このタンパク質は「DNA修復を促進する多面的タンパク質」の英語表記(pleiotropic protein promoting DNA repair)の頭文字を取って、PprAと命名された。新規遺伝子の発見とPprAタンパク質の機能解明によって、D. radioduransには、他の生物には無い独自のDNA修復機構があることが明らかになった。 3. バイオ研究試薬としての実用化 DNA鎖切断の修復は、DNAクローニングなどに使われる基本的な遺伝子工学技術である。DNAクローニングでは、DNAリガーゼというDNA修復タンパク質が汎用されており、DNAリガーゼを用いたDNAクローニングキットが国内外の試薬メーカーから多数販売されている。そこで、PprAタンパク質のDNA修復促進活性を利用し、DNAリガーゼと組み合わせることで、新しいバイオ研究試薬を開発することが検討された(図4)。その結果、2005年11月に、あるバイオ研究試薬メーカーから、PprAタンパク質を利用した高効率のDNA修復試薬「TA-Blunt Ligation Kit」が発売になった(図5)。この新製品は、従来品と比較して、修復反応終了時間が約32倍短縮され、DNA修復効率が約10倍であるという特徴を持つ。しかも、従来法では修復が難しいとされるタイプのDNA切断末端の修復に絶大な威力を発揮する。今後、このDNA修復試薬は、バイオ研究に幅広く用いられ、遺伝子診断や新薬などの開発に役立つことが期待される。 <図/表> 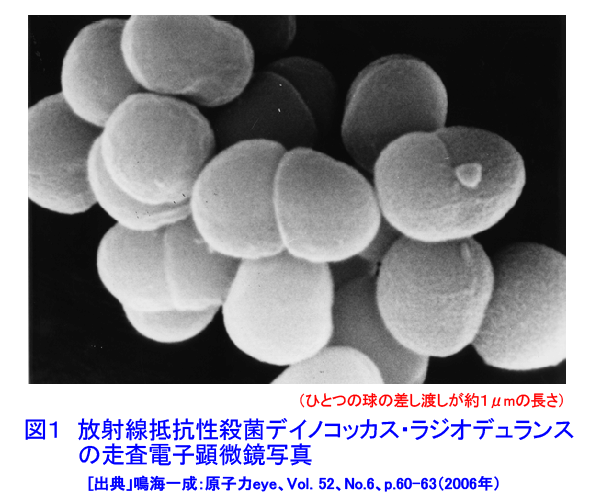

<関連タイトル> 放射線に強い微生物 (09-02-01-07) 放射線抵抗性細菌におけるDNA損傷の修復 (09-02-01-08) <参考文献> (1) Issay Narumi: Unlocking radiation resistance mechanisms: still a long way to go, Trends Microbiol. Vol.11, No.9, p.422-425 (2003) (2) Issay Narumi, Katsuya Satoh, Suzhen Cui, Tomoo Funayama, Shigeru Kitayama, Hiroshi Watanabe: PprA: a novel protein from Deinococcus radiodurans that stimulates DNA ligation, Mol. Microbiol. Vol.54, No.1, p.278-285 (2004) (3) 鳴海一成: 放射線抵抗性細菌のたんぱく質を利用した高効率DNA修復試薬の実用化、原子力eye、Vol.52、No. 6、p.60-63 (2006年)
|

