|
<解説記事ダウンロード>
<概要>
最近では、輸血する血液を放射線照射することが多い。これは、輸血する血液(graft) 製剤に含まれる供血者の白血球のひとつであるリンパ球が、患者組織中で生着、増殖し、患者組織(host)を攻撃、破壊するのを防止するためである。この病気を輸血後移植片対宿主病(PT-GVHD)と呼ぶが、有効な治療法はなく、一度発症するとほぼ95%以上死亡する。この病気に対する予防対策として輸血血液製剤への事前の放射線照射が有用な予防法として知られており、1996年日本輸血学会より放射線照射のガイドラインが示され、日本赤十字社や各医療機関において照射血供給体制が整っている。 1993年−1999年の間に発生した輸血後GVHD症例として61件が確定されているが、1981年−1986年当時にくらべ減少している。 <更新年月> 2005年02月
<本文>
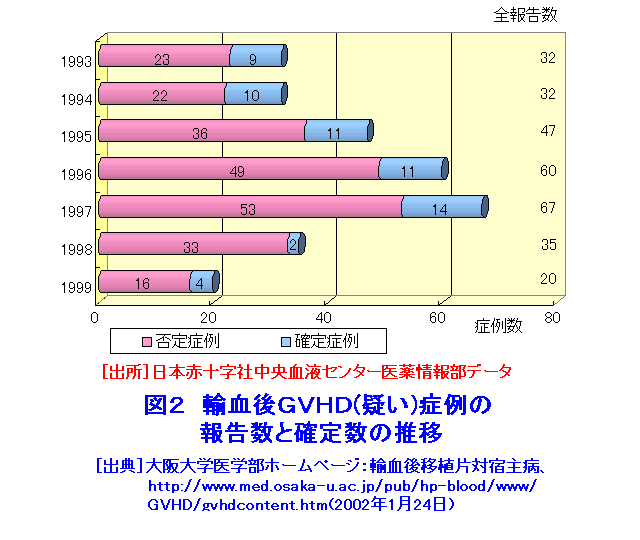
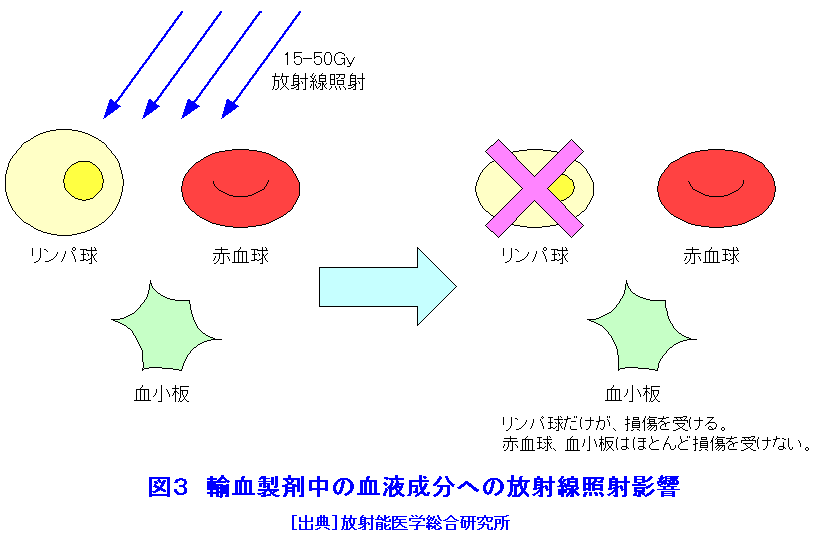
1. 輸血後GVHDとは 輸血後1−2週間後に発熱と皮膚の紅斑に始まり、肝障害、下痢、下血などが出現し、さらに白血球、赤血球、血小板がともに減少し、敗血症などの重症感染症の発症や大量の出血が起こり、輸血後3−4週で死亡することがある。以前は「術後紅皮症」として手術前後に投与された薬物や感染などが原因とみなされていたが、現在は輸血後移植片対宿主病(PT-GVHD:Post Transfusion-Graft Versus Host Disease)と考えられている。 本来私たちのからだには、自分以外のものを異物として拒絶する免疫機能が備わっている。輸血後しばらくしてから発症する理由は、輸血血液中に存在する供血者由来のリンパ球が輸血を受けた患者組織内で拒絶されずに生着し、充分に増殖してから、患者の皮膚や粘膜、肝臓、骨髄などの臓器を攻撃し症状が出現するためである。 当初は免疫の状態がよくない患者に輸血する場合にのみ、GVHD発症の危険性があると考えられていた。輸血血液中のリンパ球は、本来患者にとっては非自己であり患者の免疫細胞がこれを異物として拒絶し排除するはずである。免疫の状態がよくない患者においてはこの機能がうまく働かず、患者組織内に生着してしまうのである。ところが、そういう患者以外の場合にも、輸血後GVHDが発症することが明らかになった。 私たちのからだには血液のABO型やRh型以外にも様々な組織型があり、これを組織適合抗原(HLA:Human Leukocyte Antigen抗原、ヒト白血球抗原)というが、これが相互に似通っていると免疫担当細胞が供血者リンパ球を異物と認識しない可能性が生じ、逆に患者体内に生着したリンパ球が患者組織を異物として認識し攻撃してしまう反応、すなわちPT-GVHDが生じるのである(図1参照)。こうした場合は特殊なHLA型の組合わせの時に発症しうる。なお、こうした組み合わせをHLAの型から換算すると一般供血者からの輸血の場合は約300-900分の1、親子間の輸血では約50分の1の確率となる。この組み合わせのすべてが発症するとはいえないが、特に近親間では確率が高くなることは予想される。 1986年に日本輸血学会と日本胸部外科学会が共同で行なった調査では、1981年−1986年の6年間に行なわれた63,257件の手術で96例が発症したことが明らかになった。また、赤十字血液センターに輸血後GVHDの疑いとして報告されたもののうち、マイクロサテライトDNA多型解析によりキメリズムが確定したものは、1993年−1997年では年間約10例で推移したが、1998年には2例、1999年には4例と減少している。1993年−1999年の間に赤十字血液センターで確定した輸血後GVHD61例の患者の背景は、男性62%、60歳以上90%、輸血歴なし80%であり、93%が手術を伴った症例であった。図2に1993年−1999年の間の輸血後GVHD(疑い)症例の報告数と確定数の推移を示す。 日本に比べ外国での輸血後GVHD症例報告は極めて少ない。その理由の1つとして上記のような特殊なHLAタイプの組み合わせ頻度が少ないこともあげられる。しかし、その主な原因は、使われる血液製剤の違いが考えられる。欧米では保存血の使用が一般的であるのに対し、日本では輸血血液中のリンパ球の活きが良い新鮮血の使用頻度が高い。とくに手術当日に採血した新鮮血(この場合は血縁者からのことが多い)が好んで使われることがあげられる。 2.輸血血液の放射線照射 輸血後GVHDは今のところ有効な治療法がなく、発症してしまうと100%近い死亡率であるため、いかに未然に防ぐかが重要になる。つまりHLA型の似通った活きの良いリンパ球が多数輸血されれば、それだけ患者の体に生着して、増えていく可能性が高くなるわけであるから、他人のリンパ球が侵入するのをいかに減らすかが問題となる。まず大切なのは必要最低限の輸血を行うことである。最も安全なのは自己血輸血である。これは予定される手術などに合わせて前もって自分の血液を保存しておき輸血に使うもので、限られた場合にのみしかできない。 輸血が必要不可欠となれば、活きの良いリンパ球がたくさん含まれるような新鮮血はできるだけ使用しないこと、もちろん肉親からの輸血は避けるべきである。一般に全血を1週間保存してもその中に含まれるリンパ球の数はあまり減らないが、リンパ球の機能は、4日目頃より低下し1週間で約30分の1となる。さらに輸血の際に白血球除去フィルターを使いリンパ球の進入を防ぐのも、ある程度有用である。しかしながら、10日以上たった保存血輸血や除去フィルターを使った輸血でもGVHD発症の報告があり、これらの対策だけでは充分とは言えない。 ちなみに、赤血球、顆粒球、リンパ球、血小板といった血液成分のなかで放射線の影響を最も受けやすいのは、リンパ球である(図3参照)。そこで、輸血血液製剤にあらかじめ放射線をある程度照射することにより、混入している供血者のリンパ球に損傷を与え機能を抑えて、輸血後GVHDを予防することができる。実際、照射放射線線量が5Gy(グレイ)以上になるとリンパ球の反応増殖性がなくなる。赤血球においては、全血または赤血球濃厚液への200Gyまでの照射であれば、溶血や酸素運搬機能の変化に影響を及ぼさない。赤血球寿命も100Gy以下であれば不変である。 ただし、照射後保存して1週間以上経過すると赤血球が壊れやすくなり、カリウム濃度の増加が認められる。そのためカリウムの増加が好ましくない患者(小児、腎不全患者、大量輸血患者など)に対しては、照射後早めに少なくとも1週間以内に使用することが望まれる。血小板に対して50Gyの照射をすると、予測される値よりも輸血後の血小板数があまり増えないとされているが、生体内での寿命は不変であり照射後の輸血による血小板増加分で十分な止血効果はあるとされる。血中の蛋白質についても50Gyから100Gyの照射では電気泳動パターン上、照射前後において変化は認めない。以上のことから15Gyから50Gyの放射線照射であれば輸血本来の効果には影響を与えず、かつリンパ球の増殖能力を抑えることができるので、血液の放射線照射は、輸血後GVHDを防ぐための現在唯一の有効な手段とされている。日本輸血学会では「輸血によるGVHD予防のための血液に対する放射線照射ガイドラインIV」の中で血液製剤に対する吸収線量を15Gy-50Gyの範囲で行うように指導している。なお、米国では医療機関において医師から特定の患者に輸血の処方がなされた場合、その処方に従った製剤にたいして血液銀行で24Gyの照射が行われている。これらの点から日本赤十字社では、すべての血液パックに対して最低吸収線量として15Gyを保ち50Gyを超えない範囲で照射するとしている。このような対応措置をとった結果、輸血後GVHDと診断されたのは、1997年に14例であったものが1998年にはわづか2例(非照射血使用)にまで激減した。 3.放射線照射の問題点 放射線照射血液の輸血後の長期的な影響、つまり突然変異による発癌の問題については、自己複製能をもつリンパ球や将来白血球、赤血球、血小板になる細胞が照射によって突然変異を起こす確率、その変異した細胞が生き残る確率、さらに患者体内で拒絶されずにいる確率などをかけ合わすと、大きな危険性はないと予想される。しかしながら、ヒトでの安全性は十分確認されていない。また、15Gyから50Gyの照射線量域では、輸血用血液に混入しているウイルスなどの微生物を不活化することはできず、突然変異を誘発する可能性は否定できない。現時点でその危険性を判断することは不可能であり、長期的な評価が必要である。 1992年から、成人の心臓の手術や1500g以下の未熟児症例など1部について保険適用となったが、免疫の状態がよくない患者以外での輸血後GVHD発症の危険性を考慮すると、保険適用範囲の拡大が望まれていた。その後、1996年日本輸血学会より放射線照射の指針が示され、同年より「照射の必要があると医師が判断した場合」について保険適用が実施されるようになった。 血液専用照射装置としてセシウムを線源とするものとX線によるものがある。前者は2−3分で数単位の血液製剤に照射が可能だが、高価で放射線取り扱いの資格を有する者しか使えない。後者は同数の血液製剤への照射に10数分以上かかりX線管の交換の維持費がかかるが、使用者の資格が厳しくはない。いずれにしろ各医療施設で照射が可能か、緊急時など時間外の照射をどうするか、自施設での照射困難な医療施設への照射血の供給などの問題があげられる。なお、1993年より、国庫補助などで日本赤十字社における照射血供給体制の確立がなされはじめている。 <図/表> 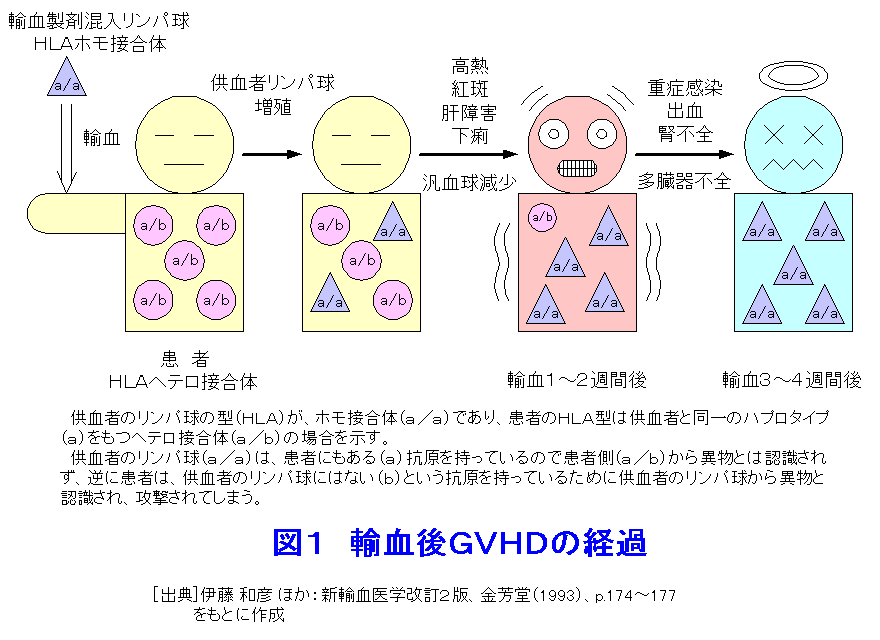
<関連タイトル> 放射線の造血器官への影響 (09-02-04-02) 白血病 (09-02-05-02) 骨髄移植 (09-03-05-02) <参考文献> (1)大阪大学医学部ホームページ:http://www.med.osaka-u.ac.jp/(2002年1月24日) (2)輸血後GVHDに対する緊急安全情報、厚生省(1997年4月) (3)日本輸血学会輸血製剤小委員会:日本輸血学会会告・輸血によるGVHD予防ための血液に対する放射線照射ガイドライン・、日輸血会誌、41(2),p.1?9(1995) (4)血液製剤の副作用の防止に関する研究班:輸血後GVHDアンケート調査報告、日本赤十字社(1991) (5)Takahasi K. et al.:Post-transfusion graft versus-host disease occuring in nonimmnosuppressed patients in Japan. Transfusion Science、12,p.281?289(1991) (6)高橋 孝善 ほか:輸血後GVHD−病態・診断・発症状況・対策−、日内会誌、82(5),p.755?760(1993) (7)岡垣 哲弥 ほか:輸血後GVHDの臨床、日本輸血学会誌、40(3),p.524?527(1994) (8)伊藤 和彦 ほか:新輸血医学改訂2版、金芳堂(1993)、p.174?177 (9)高橋 孝喜 ほか:移植片対宿主病、からだの科学、173,p.94?102(1993) (10)大戸 斉:輸血後移植片対宿主病の予防、日本輸血学会誌、40(3),p.547?551(1994) (11)Medical Practice 編集委員会(編):輸血・血液製剤療法ガイド増補版、文光堂(1995)、p.262?267 (12)野村 武夫:輸血・血液製剤療法の正しい知識、全日本病院出版会(1998)、p.70?72 (13)Ennio C. Rossi, et al.:TRANSFUSION MEDICINE, Second Edition、Williams & Wilkins(1996)、75,p.786?801 (14)伊藤 和彦:輸血後のGVHD、日本内科学会雑誌、85(6),834-838(1996) (15)森山 哲 ほか:輸血用血液製剤に対する放射線照射の条件の検討、薬学雑誌、121(4)p283-288(2001)
|

