|
<解説記事ダウンロード>
<概要>
ギリシャ時代のデモクリトスの原子論から現代の原子模型に至る原子構造解明の歴史を述べる。古代の物質観においては、アリストテレスの四元素説の方が正統とされ、原子論は異端説とされていた。18世紀末、倍数比例の法則など定量的な法則が発見されるにしたがって復活を遂げた。気体分子運動論、ブラウン運動の理論、原子スペクトルの解明などを経て現代の原子模型が確立された。 <更新年月> 1999年03月 (本データは原則として更新対象外とします。)
<本文>
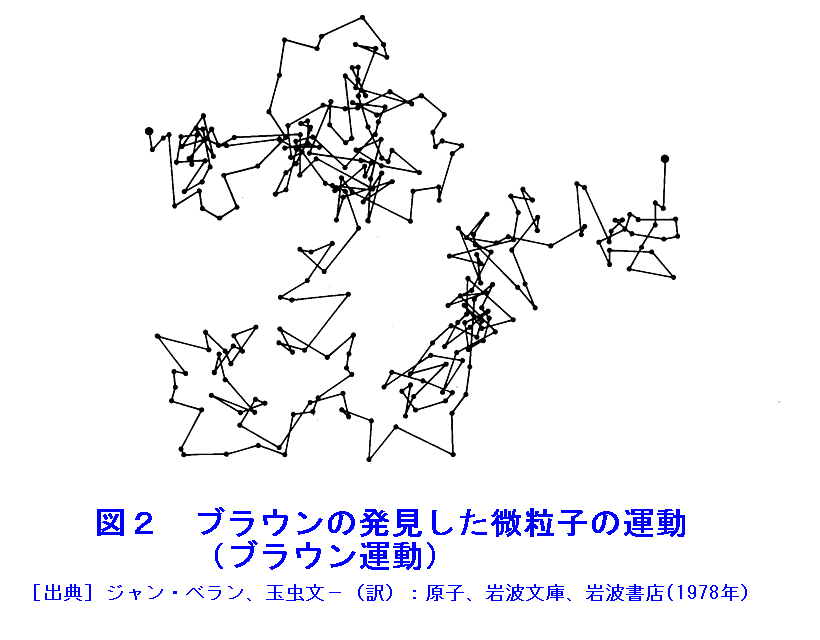
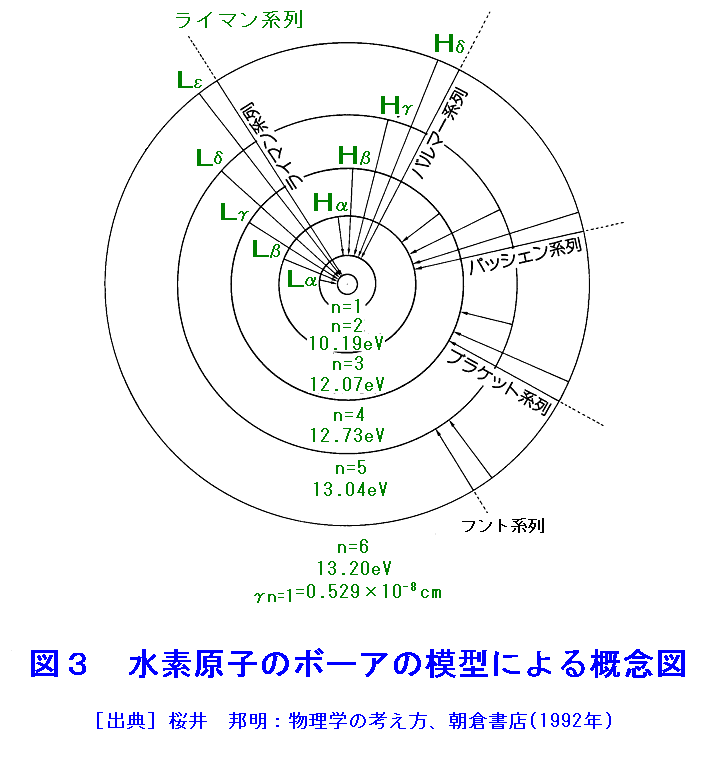
1.古代原子論 歴史に残っている最古の原子論はギリシャ時代のレウキッポス、デモクリトス(BC470〜380)によって提唱された。万物はそれ以上分割できない原子から成り、原子は空間の中を運動するという考えである。原子は多様な形を持ち、結合して世界のあらゆる物を形成する。原子の運動が物の変化をもたらすとされた。 この原子論はアリストテレス(BC384〜322)を代表とする以後の学者には必ずしも受入れられなかった。土、水、空気、火の地上の四元素に、天空のエーテルを考え、真空の存在を否定する説(何もない真空では現象は起こり得ないという考え)が主流となった。しかし原子論は異端視されながらも後世に伝えられた。 2.原子論の復活 18世紀の末から化学の研究に精密な天秤が用いられるようになった。ラボアジェ(Antoine Laurent Lavoisier、佛、1743〜1794)は、多くの実験の経験から、化学反応にあずかるすべての物質とすべての生成物質を考慮するならば、質量の変化は起らないこと(質量保存則)を発見した。また化学的に分解できない物質として33種の元素が存在することを示した。 18世紀末から19世紀にかけて、プルースト(Joseph Louis Proust、佛、1754〜1826)による定比例の法則(化合物をつくる成分元素の質量比は一定である。1799年)、ドルトン(John Dalton、英、1766〜1826)による倍数比例の法則(元素Aの一定質量と化合する元素Bの質量を異なる化合物について比較すると、簡単な整数比となる。1803年)が確立された。 これらの法則は定量的なものであり、アリストテレス以来、人々に信じられてきた定性的な四元素説では全く説明できないことが明かとなった。ドルトンは元素の一つ一つに対応させてデモクリトス流の原子を考え、これらが結合して多様な化合物を形成するという原子説によって倍数比例の法則を説明した。また原子の質量の比として原子量を定めた。ドルトンの元素記号と原子量、化合物を 図1 に示す。当時原子結合について正確な知識がなかったので、原子量は現在の値とは異なっている。 1811年アボガドロ(Amedeo Avogadro、伊、1776〜1856)は分子の概念を導入し、「等温、等圧の条件では同体積のすべての気体は同数の分子から成る。」というアボガドロの法則を提唱した。 3.熱現象の原子論による解明 気体が分子によって構成されているという説にもとづいて、気体の温度、圧力を分子の運動から説明する理論(気体分子運動論)がマクスウェル(James Clerk Maxwell、英、1831〜1879)によって考案された(1860年)。圧力は気体分子が容器壁に当たって生じ、温度は気体分子1個あたりの平均運動エネルギー(正確には回転なども含めて1自由度あたりの平均運動エネルギー)に比例する量として説明される。気体の温度、圧力、体積の関係を与える経験則であるボイル・シャルルの法則は、気体分子運動論から導かれる。 1827年、植物学者のブラウン(Robert Brown、英、1773〜1858)は、水を吸って破裂した花粉から生ずる微粒子が水中で不規則に動くことを顕微鏡下に観察した。生命に起因するものとも考えられたが、煙の粒子など粒子が微小でありさえすれば、同種の運動が観察された( 図2 参照)。この現象は、後に(1905年)アインシュタイン(Albert Einstein、独、1879〜1955)によって解析され、分子の実在の証明となった。 4.光の粒子性と波動性 光についてニュートン(lsaac Newton、英、1642〜1727)は空間(真空)を直進する性質からこれを粒子と考えたが、後にホイヘンス(Christiaan Huygens、オランダ、1629〜1695)は波動説によって光の性質をより詳細に説明し、さらにマクスウェルは光は電磁波の一種であることを理論的に導いたため、今世紀始めには光は波動であると考えられていた。 しかし今世紀に入って、高温物体から放出される光(黒体輻射)のスペクトル、金属表面に光を当てたときの電子の放出(光電効果)、光が散乱されたときの波長の変化(コンプトン効果)の研究から、光は振動数に比例するエネルギーと運動量を持った粒子としての性質を持つことがプランク(Max Planck、独、1858〜1947)、アインシュタインによって明らかにされた。すなわち光は原子レベルでのエネルギー、運動量のやりとりでは粒子としてふるまい、空間を伝播する際には波動として伝わる(粒子性と波動性の二面性を持つ)。 5.原子スペクトルと原子模型 原子は特有の振動数(波長)を持つ光(電磁波)を放光したり(輝線スペクトル)、吸収したり(吸収スペクトル)することが知られていた(これは1814年にフランホーファーがプリズムを検査している際に、太陽光線スペクトルの中に約600本の黒線を発見したことに始まる)。 1896年、ローレンツ(Hendrick Antoon Lorents、オランダ、1853〜1928)の助手のゼーマン(Pieter Zeeman、オランダ、1865〜1943)は、磁場をかけるとナトリウムから放出される光のスペクトル線が拡がることを発見し、翌年それが偏光の異なる3本の線に分裂することを確かめた。この現象はローレンツとラーマー(Joseph Larmor、英、1857〜1942)によって解析され、原子から放出される光が負の荷電粒子の運動に起因すると考えれば説明できることが示された。この負の荷電粒子の電荷と質量の比は、トムソン(Joseph John Thomson、英、1856〜1940)が発見した陰極線粒子(電子)の値に一致したので、すべての原子の中には構成要素として電子が含まれることが確実となった。この事実にもとづいて、トムソンは拡がりを持った陽電荷の球の内部にリング状に電子が配列されている原子模型を考案し、1899〜1910年にかけて原子の持つ種々の性質を理論的に説明することを試みた。原子スペクトルの他に、気体による光とX線の散乱、ベータ線の物質内での散乱と吸収が論じられた。 当時、日本でも長岡(長岡半太郎、1865〜1950)の原子模型が発表された(1904)。土星型モデルといわれるもので、中心に陽電子を持つ原子核があり、周囲をリング状に多数の電子がとり巻いている模型で、これによって化学親和力、原子価、電気分解など原子、分子に関する多くの問題を解明しようとするものであった。 6.原子核の発見とラザフォード・ボーアの原子模型 アルファ線は発見された当初、物質中を直進すると見なされていた。1906年になってラザフォード(Ernest Rutherford、英、1871〜1937)は弟子のガイガー(Hans Geiger、独、1882〜1945)、学生のマースデンとともに始めてアルファ線の散乱現象を確認した。その後、行われた一連の実験によって、稀ではあるがアルファ線の一部は原子との衝突で大きく散乱され、また軽い原子ではアルファ線が吸収されて代りに陽子が放出される現象が発見された(核反応の最初の発見)。1911年ラザフォードは、これらの現象を説明するための原子模型を提案した。この模型は中心の原子核を軌道電子がとり巻いているもので、長岡の模型と共通点があった。ボーア(Niels Bohr、デンマーク、1885〜1962)は、この原子模型において軌道電子がどんな配置をとるべきかを研究し、1913年に発表した。水素原子の場合の概念図を 図3 に示す。軌道電子は通常、原子核に最も近い軌道に入る(基底状態という。)が、光を吸収すると別の軌道に移る(励起状態)。励起状態は短時間のうちに基底状態に戻り、その際に光が放出される(図に矢印で示す)。 7.粒子性と波動性、量子力学の発展 ボーアは電子の軌道を定める際に量子条件といわれるものを導入した。これは軌道電子の運動は、それまでに知られていた力学(古典力学という。)では説明できないためである。既に光については粒子性と波動性の両方の性質があることが知られていたが、電子の軌道を定めるのに量子条件が必要となるのは、電子も光子と同じような二面性を持つためであることがわかってきた。微現的な粒子である光子、電子、陽子、中性子、原子、分子はすべて、この二面性を持つ。これらの二面性を持つ粒子のふるまいを表す力学が量子力学であり、1920年代に欧州の物理学者のさまざまな発想と討論によってその形式が整えられた。ラザフォード・ボーアの原子模型は、量子力学を用いて再構成され、現代の原子模型となった。 8.物質の階層構造 原子核の内部構造は、宇宙線や光エネルギー加速器による核反応の研究によって明らかになっていった。原子核は陽子と中性子が中間子(1935年、湯川が提唱)を互いにやりとりして結び付いている。 現在、光子、電子は内部構造を持たない点状粒子(波動性は持つ)と考えられているが、陽子、中性子、中間子は内部構造を持ち、クォークから構成されると考えられている。歴史をふり返ると、分子、原子、原子核、陽子、中性子、中間子、クォークという物質の階層構造は、技術の進歩によって新しい観測手段が提供されることによって次々と明らかになってきた。「クォークより先の階層構造の探求はどのようにして可能となるのか?」これは、今後の問題である。 <図/表> 
<関連タイトル> 超ウラン元素の発見 (16-02-02-03) 原子核の発見となったラザフォード、ガイガー、マースデンのアルファ線散乱実験と解析 (16-03-03-06) <参考文献> (1) 玉虫文一、木村陽二郎、渡辺正雄(編):原典による自然科学の歩み、講談社(1974年)、p193-360 (2) 筏 英之:百万人の化学史、アグネ承風社(1989年)、p12?16、p82-92、p110-120 (3) アイザック・アシモフ 玉虫文一、竹内敬人(訳):化学の歴史、河出書房(1967年)、p89-112 (4) ジャン・ペラン 玉虫文一(訳):原子、岩波文庫、岩波書店(1978年)p159-164、p204-206 (5) 広重 徹:物理学史1、2、培風館(1968年)、(2)p96-106、(2)p132-142 (6) F.フント 井上 健、山崎和夫(訳):思想としての物理学の歩み(上)、(下) 吉岡書店(上)1982年、(下)1983年)、(下)p277-291 (7) 物理学史研究刊行会(編):原子模型、東海大学出版会(1970年)、p183-191 (8) 物理学史研究刊行会(編):原子構造論、東海大学出版会(1969年)、p209-221
|

