|
<解説記事ダウンロード>
<概要>
核磁気共鳴画像法(MRI)は生体内の水分や脂肪の分布を検出する方法として、医学分野で発展してきたが、近年、樹木など植物組織の研究への適用が増加している。樹木の病気では、発病前の水分分布の変化が重要な意味を持つ場合が多く、MRI画像は解像度の点でも他の手法より優れている。しかしながら、T1やT2強調画像から読み取れることや、撮像パラメータの選択に必要な基礎的情報が不十分なために、適切な撮像が行われていない事例も見受けられる。ここでは、MRIによる樹木内部の水分分布および病変部の検出について、撮像事例を紹介しながら解説し、人間の生体を対象とした撮像法を植物にそのまま適用できるのかどうかなど、適用上の問題点を指摘した。 <更新年月> 2007年08月
<本文>
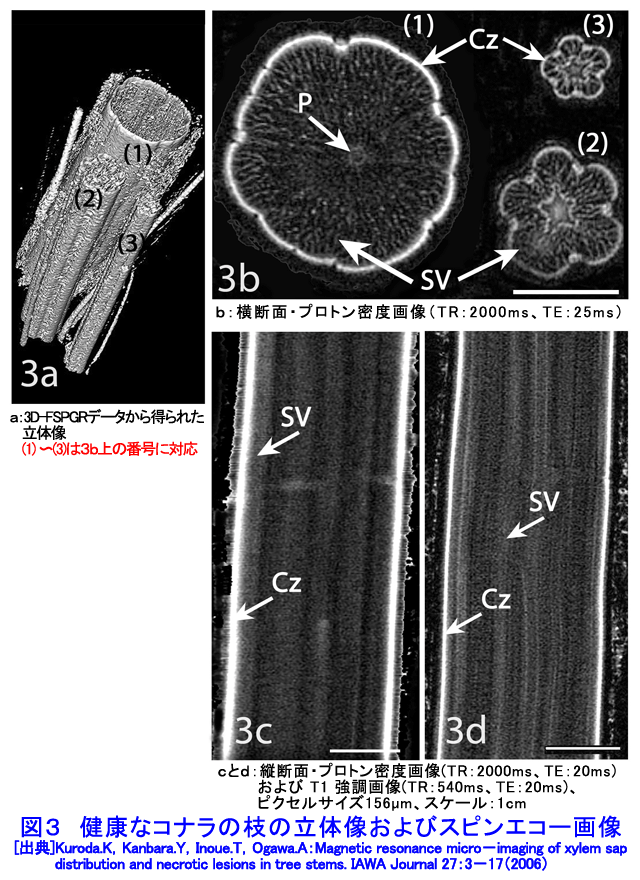
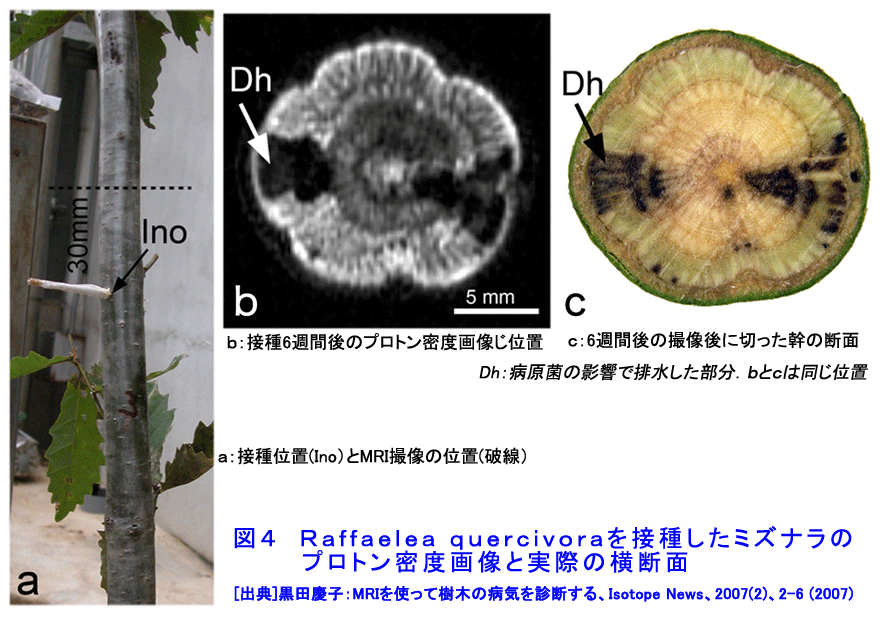
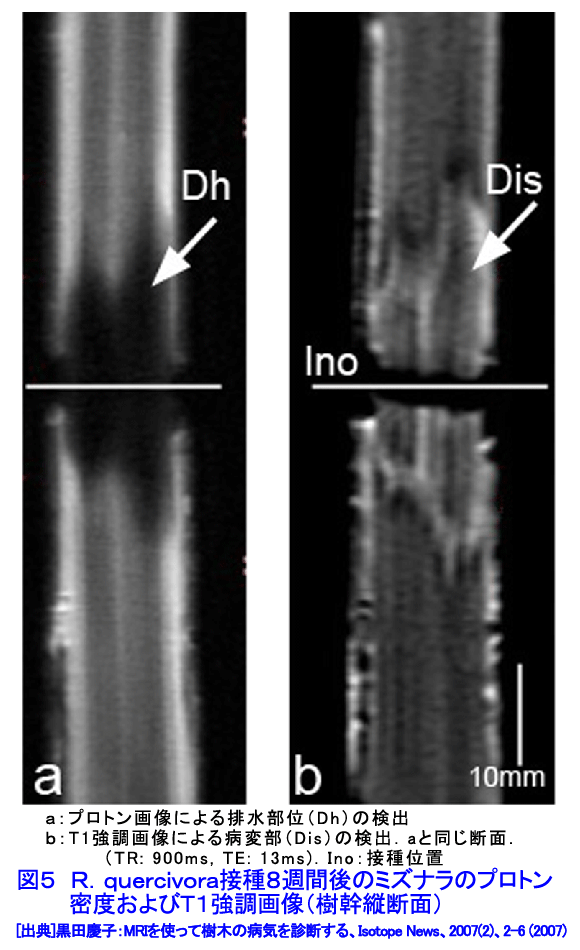
1.MRIによる樹木の水分分布の観察 樹木に病気を起こす微生物としては菌類が多く、その他に細菌や線虫などがある。感染後に幹の内部で起こる水分の減少や細胞の壊死などの変化を、葉の変色などの病徴が発現する前に検出することは非常に困難であり、非破壊的な観察手法の活用が求められてきた。これまでに超音波、マイクロ波、軟エックス線などの応用例はあるが解像度が低いことから、利用はあまり進んでいない。一方、核磁気共鳴画像法(MRI)は水分分布の検出精度が高く、適用例は近年増えつつある。しかしながら、植物への適用については原理の概論程度の解説書しかなく、撮像技術として定まったものがまだないため、予備実験をして、撮像条件を決めるところから始めなければならない。 1.1 樹木の撮像手順 日本では、臨床用MR装置で人間以外の生物を撮像するのは制度上難しく、研究専用機が設置されている施設での撮像が主になる。ここでは3Tesla(30000ガウス)のMR imaging system(Signa VH/i 3.0 T,General Electric Medical Systems;岩手医科大学超高磁場MRI研究施設)を用いた事例で、樹木の中の水分分布を検出するための撮像手法について説明する。 樹木を生きたまま撮像するには、鉢植えにしたものをポリ袋で覆って装置に持ち込むことになるので、樹高2m程度までの若木に限定される。幹や枝を切断しても良い場合は、直径の大きい樹木でも撮像できるが、切断部から水分が蒸発しないように両端を被覆して装置に入れる。スピンエコー(SE)やグラディエントエコー(FSPGR)などいくつかのシークエンスを組み合わせると1試料の撮像に40分〜1時間程度かかり、半日に5試料程度の撮像が可能である。 FOV(Field of View)は60、80、200mmなど、2次元のSEシークエンスでは、スライスの厚さは0.8〜5.0mmとした。また、厚さ0.8mmで120〜200セクションからなるFSPGRシークエンスのデータを用いて3次元の解析を行った。画像の解析には、OsiriXなどフリーソフトも利用できる。 画像の解像度は、 FOV 解像度(ピクセルサイズ)=−−−−−−− イメージサイズ で算出される。FOVが60mm、イメージサイズが512μmの場合、解像度は117μmである。光学顕微鏡より一桁以上低いが、樹木の中の水分分布を検出する手法としては最も精度が高い。 1.2 樹木の解剖学的特徴とMRIでみた健康な樹木の水分分布 針葉樹のアカマツ(Pinus densiflora Sieb. et Zucc.)および広葉樹のコナラ(Quercus serrata Thunb.)の幹横断面の光学顕微鏡画像を図1に示す。樹木では、生きている細胞内の水分以外に、木部(樹皮以外の木材の部分)にある筒状の通道組織を満たしている「木部樹液」と呼ばれる水分が存在する。この水は人間の血液に匹敵するほど重要で、水分欠乏の樹木は罹病しやすいことが知られている。針葉樹では、木部の大部分は仮道管(図1aのTr)と呼ばれる通道組織からなり、一方、大半の広葉樹では分布密度の低い道管(図1bのLVとSV)が通道を主に担う。健康な樹木の木部樹液は、ほとんど混入物のない水である。根で吸い込まれた水は、葉から水が蒸発する(蒸散)際に発生する張力と水分子の凝集力によって幹の中を上昇し、梢の先まで到達することができる。 プロトン密度画像およびT2強調で得られた画像では、水で満たされた通道組織は図2と図3に示すように、白く見える。アカマツの木部には直径20〜30μmの仮道管がぎっしりと集まっており(図1b、Tr)、若い幹ではほとんど全範囲で水分が上昇しているため、画像全体が白く見える(図2、CX)。ただし、外側の年輪より内側の年輪がやや暗く、幹の部位により水分量が違うと推測される。また、年輪界の黒く見える部位(図2、LW)では、仮道管の水が失われて空洞になっており、機能していない。コナラでは、大径道管の直径が300μm程度あるので(図1b、LV)、中に水が入っていれば一本ずつの管の断面が見えるが、夏季には空になっていることが多く、図3の画像では大径道管は見えていない。小径の道管の直径は100μm以下で(図1b)、MR画像のピクセルサイズ(画像解像度)より小さいため、いくつか集まった部分が白く塊状に見える(図3b、SV)。また、広葉樹の幹では、水の入っていない木部繊維(図1b、F)が多数分布するため、プロトン密度画像では、針葉樹よりも黒く見える部分が多い。細胞分裂を盛んに行っている形成層帯(図2、図3、Cz)では、生きている細胞が内容物を持っているため白い帯状に見える。樹液のみの部分よりもMR信号が強いことから、水以外の物質が影響している可能性もある。 2.MRIを用いた病変部の観察 2.1 罹病木のMRI画像 樹木の幹では、感染や傷害を受けると部分的に水分が抜けて気体に置き換わる現象(ドライゾーンの形成)がある。このような部分は乾燥しており、プロトン密度画像やT2強調画像では暗く見える。病原体を接種してから7〜10日間隔で撮像すると、樹液流動阻害の進行を非破壊で追跡することができる。図4は、近年日本各地でナラ類樹木に集団枯死を起こしている糸状菌Raffaelea quercivora Kubono et Shin. Itoをミズナラ(Quercus Crispula Blume)に接種した例である。SEシークエンスでは、TR=4000msまたは2000ms、TE=21〜22msで撮像した場合に良好なコントラストの画像が得られている。 6週間後の撮像(図4b)のあとで切断した横断面では、病原菌の分布範囲が褐色に変色しているのが肉眼で認められ、変色範囲の道管は排水して空洞になっている(図4c、Dh)。この変色範囲はプロトン密度画像の暗い部分(図4b、Dh)に完全に一致する。画像から判断した排水部位と解剖の結果との対応が確認されたことから、樹液流動阻害を起こす萎凋病の研究にMRIが有用であることがわかった。 2.2 T1およびT2強調画像 T1強調画像は、医学分野のMRI診断で最も一般的に使用されることから、植物の撮像でもよく使われている。菌を接種したミズナラ樹幹で、プロトン密度画像やT2強調画像で暗く見えた排水部位は、T1強調画像(TR:540ms、TE:20ms)では白く見える(図5a、b)。これは菌が分布し、宿主細胞が菌の影響により壊死した部位に対応する。人体ではT1強調では脂肪やタンパクを多く含む部位がわかり、病変部の検出に利用すると説明されているが、人体の場合の解釈を樹木に適用できるかどうか検証されていないので、同じ成分が含まれているとは断定できない。現時点では図5bの白い部分(Dis)は、菌あるいは樹木の代謝により生成した物質の蓄積があるのだろうと推測される。このように、プロトン密度およびT2強調画像で樹幹の中の水分分布を検出するだけでなく、T1強調画像を用いて組織の壊死あるいは病変部を検出することができる。T1強調画像で検出される物質の同定については、今後の研究の課題である。 2.3 撮像および画像解釈の問題点 海外では2000年ごろから植物への適用例が増えつつあり、研究用の大型MRI装置を設置している大学等も増加している。ただし、学術雑誌に掲載された論文には不鮮明な画像が多く含まれ、パラメータや撮像シークエンスの選択についてきちんと記述していない例や、画像の解釈に問題のある論文もある。たとえば、T1強調画像を用いて水分分布を論じている例である。T1強調画像はコントラストが高めになるので(たとえば図3cと3dを比較)、視覚的効果があるため使用するのかもしれない。確かに、健全な植物ではプロトン密度やT2強調画像とT1強調画像の差が少ない傾向があるが(図3)、罹病樹木の画像(図5)では、T1強調画像は明らかにプロトン密度画像と異なり、水分の少ない病変部を白く示している。画像の解釈に関する問題を認識している研究者は少数であり、論文査読者が対応できないケースが多いのではないかと推測される。今後、医学分野からの指導や植物研究用の技術指導書が早急に必要とされている。 <図/表> 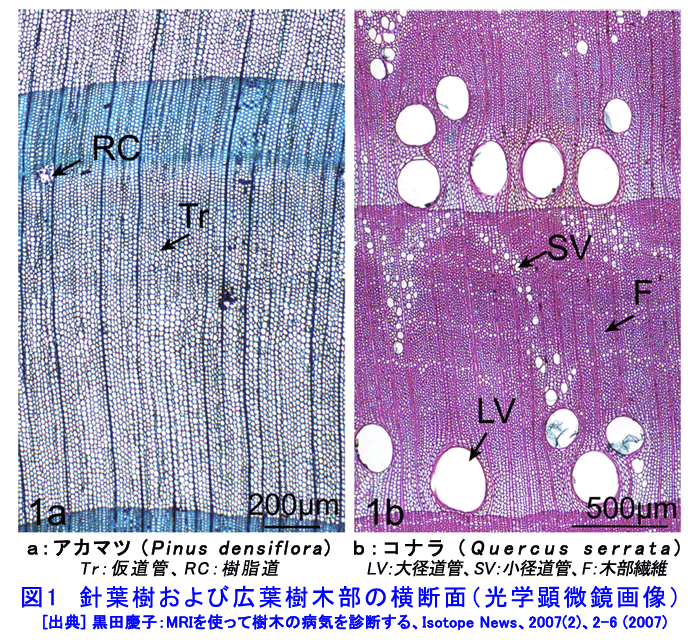

<関連タイトル> 核磁気共鳴イメージング(MRI)の原理と応用 (08-02-01-05) <参考文献> (1)Bucur V.:Nondestructive characterization and imaging of wood. Springer,Berlin,Heidelberg(2003) (2)Kuroda.K,Kanbara.Y,Inoue.T,Ogawa.A:Magnetic resonance micro-imaging of xylem sap distribution and necrotic lesions in tree stems. IAWA Journal 27:3-17(2006) (3)Manion PD,Griffin DH:Resistance in aspen to Hypoxylon canker. In:Defense mechanisms of woody plants against fungi. Blanchette & Biggs(Eds.)308-320,Springer,Berlin,Heidelberg(1992) (4)Zimmermann MH:Xylem structure and the ascent of sap. Springer,Berlin,Heidelberg,New York(1983) (5)Kuroda K:Responses of Quercus sapwood to infection with the pathogenic fungus of a new wilt disease vectored by the ambrosia beetle Platypus quercivorus. J. Wood Sci. 47:425-429(2001) (6)Rosset A, Pysher L,Spadola L,Ratib O OsiriX Medical Imaging Software. http://www.osirix-viewer.com/ (7)NessAiver.M(著)、押尾晃一、百島祐貴(訳): 図解 原理からわかるMRI、医学書院(1998年1月) (8)黒田慶子:森林の健康や生物被害に関する解説 (9)黒田慶子:MRIを使って樹木の病気を診断する、Isotope News、2007(2)、2-6 (2007)
|

